Nghiên cứu khoa học
Động lực học nước sinh học và Entropy: Nguồn gốc vật lý sinh học ung thư và các bệnh khác
Một nghiên cứu khoa học về nước sinh học và nguồn gốc của bệnh tật, được Koro tạm dịch cơ bản từ báo cáo nước ngoài có tựa đề: "Biological Water Dynamics and Entropy: A Biophysical Origin of Cancer and Other Diseases"
Tóm tắt: Bài báo này giả định rằng cấu trúc của nước bị thay đổi bởi các phân tử sinh học cũng như bởi các thực thể gây bệnh như một số ion solvat hóa, và đến lượt nó, động lực và cấu trúc của nước ảnh hưởng đến chức năng của các tương tác giữa các phân tử sinh học. Mặc dù những thay đổi về cấu trúc và động lực học là tinh vi, nhưng chúng làm xáo trộn một hệ thống cân bằng đủ để tạo điều kiện thuận lợi cho dịch bệnh. Chúng tôi đề xuất rằng sự gián đoạn của động lực nước giữa và trong các tế bào là nguyên nhân dẫn đến nhiều tình trạng bệnh tật. Chúng tôi khảo sát những tiến bộ gần đây trong từ sinh học, sinh học nano, khoa học chất keo và giao diện, khuếch tán, đông đúc nội bào và tự lắp ráp phân tử. Nước giữa các pha và sức căng bề mặt tế bào, thường được duy trì bởi các sunfat sinh học ở bề mặt màng, bị tổn hại bởi các yếu tố gây căng nước bề mặt ngoại sinh như nhôm cation, với các hậu quả bao gồm tính kỵ nước cục bộ lớn hơn, tăng sức căng của nước và kéo dài giữa các pha. Kết quả cuối cùng là “độ cứng” lớn hơn trong chất nền ngoại bào và trạng thái ung thư “mềm” hoặc trạng thái thoái hóa thần kinh “mềm” trong tế bào. Giả thuyết của chúng tôi cung cấp cơ sở để hiểu tại sao rất nhiều bệnh vô căn ngày nay có tính rập khuôn và đa nguyên nhân cao.
Từ khóa: nhôm; Sự hỗn loạn; chất độc hại; chất gây ung thư; proteoglycan heparan sulfat; ung thư vú; tác dụng kỵ nước; giữa các giai đoạn; ứng suất nước giao thoa; ung thư hạch; nước nhiễm từ; bệnh ung thư buồng trứng; bệnh ung thư tuyến tụy; ung thư phổi; các cụm nano nước.
Mã PACS: 87.19.xj; 87.19.xr; 87.19.xv; 87,19xw; 87.19.xb; 87,19xp; 03,75.Hh; 03,75.Kk; 42,50.Gy; 87,15.B; 03,75.Lm; 87,15.N; 75.10.-b; 75,78.-n; 82,70.Uv; 36,40.Wa; 68,35.Rh; 74,25.fc
1. Giới thiệu: Rối loạn chức năng phân tử sinh học là Nguyên nhân hay Dấu hiệu sinh học của bệnh?
Các tài liệu nghiên cứu y học rộng lớn chứa đựng nhiều tài liệu về những thay đổi rối loạn chức năng trong cấu trúc và hoạt động phân tử sinh học được thấy trong các bệnh mãn tính và truyền nhiễm. Các hiện tượng ở cấp độ phân tử được mô tả bao gồm kích hoạt gen không thích hợp và tổng hợp protein thúc đẩy sự phân chia không kiểm soát của tế bào ung thư, sự chuyển hướng của quá trình biểu hiện gen tương tự này nhằm tăng sinh vi rút lây nhiễm và đám rối protein beta-amyloid đặc trưng của bệnh Alzheimer. Thông tin chi tiết về các bệnh riêng biệt khác nhau, nhưng đặc điểm chung của các cơ chế phân tử được cung cấp cho tất cả chúng là nhấn mạnh vào vai trò của các đại phân tử và các chất nền hoặc phối tử không chứa nước của chúng, mà ít hoặc không chú ý đến nước, phân tử phong phú nhất trong cơ thể. và điều cần thiết nhất cho mọi dạng sống. Trong bài báo này, chúng tôi trình bày một quan điểm khác về căn nguyên bệnh đặt nước ở trung tâm của giai đoạn. Chúng tôi đề xuất rằng nguyên nhân chính của chứng viêm và bệnh tật là sự phá vỡ cấu trúc nước bình thường giữa và bên trong tế bào, sau đó làm phát sinh những thay đổi đại phân tử bệnh lý được báo cáo trong y văn. Chúng tôi đưa ra một giả thuyết chi tiết xác định một tuyến đường dẫn nước đến bệnh lý và xem xét những tiến bộ gần đây trong sinh học từ tính, sinh học nano cũng như khoa học chất keo và giao diện hỗ trợ ý tưởng của chúng tôi.
Sự gián đoạn trong nước và cấu trúc phân tử sinh học mà chúng ta thảo luận ở đây thường liên quan đến sự gia tăng entropi, trong đó từ entropy được sử dụng theo nghĩa nhiệt động lực học thông thường là “rối loạn” hoặc “năng lượng không có sẵn cho công việc hữu ích.” Trái ngược với entropy của hệ thống, chúng tôi hướng sự chú ý đến entropy cấu trúc phân tử của nước và các phân tử sinh học. Do đó, chúng tôi không muốn nhầm lẫn việc sử dụng từ entropy với khái niệm entropy sinh học, như được định nghĩa bởi Oller [1], mặc dù entropy cấu trúc phân tử về mặt logic sẽ là một thành phần của mô hình phân cấp lồng nhau của tổ chức sinh học, có lẽ cung cấp có nghĩa là cho cả năng lượng và dòng thông tin.
Chúng tôi bắt đầu quan điểm “dựa trên nước” về căn nguyên của bệnh trong Phần 2 dưới đây, nơi chúng tôi thảo luận ngắn gọn về những phát triển chính trong thiết bị chẩn đoán và phân tích đã cho phép các nhà khoa học đo lường các đặc tính của nước cần thiết cho sự sống, để có được bằng chứng về vai trò quan trọng của nước trong việc xác định và duy trì cấu trúc và chức năng bình thường của đại phân tử, và để phát hiện sự khác biệt giữa cấu trúc nước trong mô bình thường và mô bệnh. Những phát hiện này cho thấy sự phá vỡ cấu trúc sinh học của nước là nguyên nhân gây ra bệnh lý. Thật vậy, trong một bài đánh giá trước đó, chúng tôi đã đề xuất căng thẳng nước giao diện ngoại sinh (EIWS), một sự gia tăng bệnh lý của sức căng nước tại các bề mặt sinh học như bề mặt tế bào, như là giai đoạn ban đầu trong một con đường phổ biến dẫn đến các hiện tượng viêm và huyết khối, bao gồm đột tử [2 ]. Dựa trên đánh giá trước đây của chúng tôi [2], chúng tôi mô tả trong Phần 3 “giả thuyết trung tâm” của chúng tôi rằng EIWS gây ra một chuỗi các sự kiện trong không gian ngoại bào và nội bào có thể dẫn đến nhiều phản ứng bệnh lý khác nhau. Phần 4–6 là khảo sát tài liệu mở rộng nhằm cung cấp và hỗ trợ cho từng bước trong con đường đề xuất của chúng tôi đến các trạng thái bệnh ung thư, truyền nhiễm và thần kinh. Cụ thể, Phần 4 trình bày những phát hiện gần đây về cấu trúc và tính chất của nước sinh học, được duy trì bởi sunfat sinh học trên bề mặt màng và bởi từ trường yếu. Phần 5 xem xét các tác động phá vỡ nước của các yếu tố gây ra căng thẳng nước ngoại sinh giữa các môi trường, trong đó nhấn mạnh đến cation nhôm, có liên quan đến bệnh ung thư vú và bệnh Alzheimer. Phần này cũng đề cập đến các tổn thương ngoại bào và nội bào gây ra bởi sự mất kết nối giữa chất nền ngoại bào và bộ xương tế bào, cũng như các tác động bất lợi trực tiếp bổ sung của các yếu tố gây căng thẳng nước giữa các bề mặt đối với môi trường nội bào. Phần 6 khảo sát việc áp dụng EIWS đối với các bệnh cụ thể, bao gồm ung thư vú, bệnh thần kinh và bệnh truyền nhiễm. Phần 7 gồm những nhận xét và kết luận của chúng tôi.
2. Bối cảnh lịch sử: Những tiến bộ trong việc đo lường các thuộc tính nước có liên quan đến sinh học
Tính dẫn điện của các hệ thống nước trong cơ thể như huyết tương và tế bào thần kinh là một hiện tượng được chấp nhận rộng rãi ngày nay. Bên cạnh đó, từ thế kỷ 19, người ta đã biết rằng dòng điện tạo ra từ trường, và gần đây điều ngược lại cũng được phát hiện là đúng: từ trường chuyển động có thể làm phát sinh dòng điện trong các vật dẫn gần đó. Tuy nhiên, những phát hiện khoa học từ sinh học vẫn chưa được tin cậy cho đến những năm 1960, khi các từ kế có độ nhạy đủ cao cuối cùng đã được phát triển để cho phép đo từ trường của tim (yếu hơn khoảng một triệu lần so với từ trường của Trái đất) và thậm chí còn yếu hơn từ trường của các các cơ quan và mô [3,4]. Từ kế nhạy và được sử dụng rộng rãi nhất hiện nay là thiết bị giao thoa lượng tử siêu dẫn (SQUID), chứa các điểm nối Josephson, bao gồm hai chất siêu dẫn được ngăn cách bởi một lớp vật liệu cách điện mỏng mà qua đó có thể diễn ra quá trình đào hầm lượng tử. Với sự trợ giúp của SQUID, các nhà nghiên cứu đã có thể hiểu sâu hơn về cách di chuyển của động vật di cư [5] và liệu pháp điện từ xung có thể giúp chữa lành xương gãy [3]. SQUID cũng hỗ trợ các nghiên cứu về nước sinh học từ hóa như được thảo luận trong Phần 4 dưới đây.
Sự phát triển của SQUID để đo từ trường rất yếu, có liên quan đến sinh học đã song song với sự phát triển của chụp cộng hưởng từ (MRI), sử dụng từ trường năng lượng cao hơn nhiều trong dải tần số vô tuyến như một công cụ chẩn đoán y tế. MRI phụ thuộc vào nồng độ cao của nước trong các mô cơ thể, vì nước là nguồn chính của các hạt nhân 1H liên kết với hoặc chống lại từ trường được áp dụng. Sự khác biệt về thời gian giãn của proton nước và mật độ xoay làm cơ sở cho độ phân giải không gian và độ tương phản của hình ảnh MRI. Kể từ khi phát minh ra MRI vào đầu những năm 1970 [6], các nghiên cứu đã chứng minh tính hữu ích của nó trong việc phân biệt tế bào khối u với tế bào không phải khối u, với nước xuất hiện ít cấu trúc hơn trong tế bào khối u [7-9]. Các nghiên cứu cộng hưởng từ proton cũng cho thấy những thay đổi đáng kể trong cấu trúc nước tế bào trong quá trình nguyên phân bình thường [10–12]. Mặc dù MRI được sử dụng rộng rãi như một công cụ chẩn đoán y tế, những thay đổi trong cấu trúc nước sinh học được chỉ ra bởi các phép đo MRI dường như được nhiều người coi là dấu hiệu hơn là nguyên nhân có thể gây ra các bệnh đang được nghiên cứu. Điều trớ trêu này đã được Oschman [3] nhận xét nhưng dường như không được các nhà nghiên cứu y học “chính thống” chú ý.
Ngoài những tiến bộ trong phép đo từ trường yếu và chẩn đoán MRI, những phát triển gần đây trong các kỹ thuật quang phổ khác nhau đã cho phép các nhà nghiên cứu thăm dò các đặc tính của các phân tử nước gần với các bề mặt ưa nước và kỵ nước, bao gồm cả vật liệu vô cơ và sinh học. Tán xạ nơtron không đàn hồi và bán đàn hồi [13,14], quang phổ tạo tần số tổng hợp [15], quang phổ phân ly hồng ngoại (IRPD) [16] và quang phổ điện môi băng rộng [17] bao gồm một vài ví dụ về các công cụ phân tích mới hơn này. Các kết quả chính của những nghiên cứu này, cho thấy sự khác biệt đáng kể về cấu trúc giữa nước lỏng giữa các bề mặt và nước dạng khối, cũng như sự phong phú của nước giữa các bề mặt trong các hệ thống sinh học, được thảo luận trong Phần 4 của bài viết này.
Sự phát triển phân tích thứ tư đáng chú ý ở đây bao gồm các kỹ thuật như quang phổ điện môi băng rộng, các phương thức tán xạ nơtron khác nhau và quang phổ hấp thụ terahertz động học (KITA) cho phép nghiên cứu các hệ thống sinh học trên quy mô thời gian xuống đến pico giây và do đó có thể cung cấp cái nhìn sâu sắc về mối liên hệ giữa nước và chuyển động phân tử sinh học [18–25]. Trong một cuộc điều tra KITA gần đây về chất nền peptit liên kết với metalloproteinase ở người, không có kết luận nào về việc chuyển động của nước có trước hay sau chuyển động của enzym [23]. Ngược lại, nhiều nghiên cứu về sự gấp khúc của protein và về các protein và axit nucleic đi qua nhiệt độ chuyển thủy tinh của chúng (nhiệt độ dưới nhiệt độ mà đại phân tử ngậm nước cho thấy chuyển động bị hạn chế cao và ít hoặc không có hoạt tính sinh học) thường chỉ ra rằng sự thay đổi nhanh hơn trong nước cục bộ cấu trúc trước những thay đổi cấu trúc chậm hơn, chính của các đại phân tử [17–36].
Dựa trên dữ liệu từ các nghiên cứu nhiệt độ chuyển tiếp và gấp khúc của thủy tinh, một số nhà nghiên cứu đã tuyên bố rằng các chuyển động của phân tử sinh học là “nô lệ” cho những thay đổi trong cấu trúc nước [17,36], mặc dù những người khác tin rằng thuật ngữ này không thừa nhận đầy đủ ảnh hưởng của đại phân tử trên mặt nước xung quanh [14,37]. Bản chất phức tạp và thời gian của tương tác nước-đại phân tử lẫn nhau này được minh họa rõ ràng trong các thí nghiệm của Fuxreiter et al. [38], người đã chỉ ra rằng sự phân bố của nước hydrat hóa gần DNA hiển thị các biến thể phụ thuộc vào trình tự cơ sở, do đó kiểm soát số lượng phân tử nước được giải phóng từ một trình tự nhất định khi chuyển đổi từ phức hợp lỏng sang phức hợp chặt chẽ. Tuy nhiên, ngay cả những nhà điều tra phản đối việc “nô lệ hóa” như một thuật ngữ mô tả cho những hiện tượng này đã lưu ý rằng “có thể không có“ sự nô dịch hóa ”, nhưng nước hydrat hóa phải là động lực trong liên kết động” [14].
Bằng chứng cho thấy những thay đổi trong cấu trúc nước dẫn đến hoặc xác định những thay đổi bình thường trong cấu trúc protein và DNA dẫn đến câu hỏi liệu những thay đổi khác trong cấu trúc nước có thể gây ra những thay đổi bệnh lý được quan sát thấy trong các đại phân tử này trong quá trình phát triển bệnh hay không. Trong phần còn lại của bài báo này, chúng tôi coi bằng chứng rộng rãi hỗ trợ kết luận rằng sự phá vỡ cấu trúc nước sinh học thực sự là một nguyên nhân chứ không chỉ đơn thuần là một dấu ấn sinh học của bệnh tật.
3. Luận văn trung tâm: EIWS thúc đẩy những thay đổi ngoại bào và nội bào đối với bệnh tật
Luận điểm trọng tâm là căng thẳng nước giao diện ngoại sinh (EIWS), bằng cách phá vỡ cấu trúc nước sinh học, bắt đầu một loạt các sự kiện trong không gian ngoại bào và nội bào dẫn đến rối loạn và bệnh tật, chẳng hạn như bệnh lý thần kinh, nhiễm trùng, ung thư và tử vong. Những thay đổi gián đoạn xảy ra trong khoảng pha nước, vùng gần bề mặt phân tử sinh học, nơi cấu trúc và tính chất của nước khác với cấu trúc và đặc tính của nước dạng lỏng. (Một cuộc thảo luận chi tiết về sự phân biệt giữa giao diện / giữa các pha được cung cấp bởi Geckeler và cộng sự. [39].) Phân tầng được đề xuất đối với bệnh lý bao gồm các bước sau:
(a) Các cấu trúc nước có khả năng sống trong dung dịch nước, thường được duy trì bởi từ trường yếu và các proteoglycan heparan sulfat (HSPG) trang trí bề mặt màng tế bào, bị phá vỡ bởi các tác nhân gây căng thẳng nước ngoại sinh như các cation nhôm.
(b) Sự gián đoạn này dẫn đến tính kỵ nước cục bộ, không mong muốn, tăng sức căng của nước và “làm mềm” màng. Ngoài ra, nhôm cation liên kết với các HSPG trên bề mặt tế bào bằng cách trung hòa điện tích và do đó phá vỡ phức hợp màng HSPG kết nối các thành phần chất nền ngoại bào với bộ xương nội bào.
(c) Sự tách rời kết quả của bộ xương tế bào khỏi màng sinh chất gây ra một số hậu quả bất lợi, bao gồm suy giảm khả năng dẫn điện của bộ xương và vi ống và tái định hướng của bộ xương tế bào về phía nhân tế bào, có thể đẩy nhanh quá trình nguyên phân bệnh lý của bệnh ung thư.
(d) Ngoài ra, sự xâm nhập của yếu tố gây căng thẳng nước giữa bề mặt (ví dụ, cation nhôm) vào tế bào phá vỡ cấu trúc nước nội bào, dẫn đến phản ứng protein không mở, phản ứng DNA không mở và sản xuất ROS dư thừa.
Việc nhấn mạnh vai trò trung tâm của nước, phân tử phong phú nhất trong cơ thể, đánh dấu sự khởi đầu từ chất nền sinh học phân tử điển hình, chất thụ thể protein và sự kết hợp cơ sở di truyền, Watson-Crick, cách tiếp cận “khóa và chìa khóa” để hiểu ung thư và những căn bệnh khác. Các phần sau đây khảo sát tài liệu rộng rãi cho thấy các tính chất đặc biệt của nước nhiễm từ được tìm thấy trong các hệ thống sinh học và hỗ trợ từng bước trong trình tự đề xuất từ EIWS đối với các rối loạn, bệnh tật, ung thư và tử vong.
4. Cấu trúc nước sinh học trong không gian ngoại bào và nội bào
Bước đầu tiên trong hành trình EIWS hướng tới các bệnh lý ngày càng nghiêm trọng là xem xét nghiên cứu gần đây liên quan đến cấu trúc của nước sinh học. Trong hệ thống sinh học, sự sắp xếp của các phân tử nước bị ảnh hưởng bởi sự tương tác với các chất tan nhỏ (ion, khí hòa tan, phân tử nhỏ), bề mặt mở rộng của các tổ hợp hoặc phân tử sinh học lớn (protein, bề mặt màng tế bào, v.v.), và điện từ trường yếu. Theo một cách gần đúng đầu tiên, các cấu trúc nước bình thường được duy trì phần lớn nhờ tương tác với các bề mặt phân tử sinh học và trường điện từ, cho phép các mạng mở rộng cho độ dẫn điện tử và proton. Tuy nhiên, như đã thảo luận trong Phần 5, cation nhôm và nhiều tác nhân gây căng thẳng nước khác (ví dụ: thủy ngân, chì, glyphosate, amoniac, fomanđehit, asen, florua, v.v.) là những chất hòa tan nhỏ có thể làm gián đoạn mạng mở rộng về độ dẫn điện, vì vậy hãy hiểu cách các chất hòa tan nhỏ tác động đến cấu trúc nước cục bộ là điểm khởi đầu cần thiết.
4.1. Tương tác với các chất hòa tan nhỏ
Năm 1888, Hofmeister báo cáo kết quả nghiên cứu thực nghiệm của mình về khả năng kết tủa hoặc hòa tan protein của các loại muối khác nhau trong dung dịch nước [40]. Dựa trên những nghiên cứu này và những nghiên cứu tiếp theo, nhiều ion đã được phân loại là “kosmotropes” hoặc “chaotropes” tùy thuộc vào tác động “tạo cấu trúc” hoặc “phá vỡ cấu trúc” của chúng trên các phân tử nước xung quanh [41–44]. Các ion có mật độ điện tích cao và độ phân cực thấp, chẳng hạn như Li + và F−, có xu hướng là dạng kosmotropes, trong khi các ion có mật độ điện tích thấp hơn và độ phân cực cao, chẳng hạn như Cs + và SCN−, có xu hướng là dạng thù hình.
Trong bài báo này, chúng tôi tập trung vào ảnh hưởng của hai ion kosmotropic mạnh, SO4−2 và Al3 +, đối với cấu trúc nước sinh học. Các tác động bất lợi của Al3 +, một chất gây căng thẳng nước giao diện ngoại sinh tinh túy, được đề cập rộng rãi trong Phần 5 và 6 dưới đây. Ngược lại, như đã thảo luận trước đó [2], việc làm giảm sức căng bề mặt có lợi của sulfat và nâng cao thế zeta của các phân tử lơ lửng và tế bào trong máu về giá trị âm hơn được tối đa hóa ở khoảng 0,5 mM, nồng độ sulfat trong huyết tương ( thế zeta của một hạt keo, một đại lượng liên quan chặt chẽ đến điện tích bề mặt thực của nó và số lượng và loại ion có trong môi trường mà nó lơ lửng, có thể được xác định dễ dàng bằng cách đo tính linh động của hạt trong môi trường dưới ảnh hưởng của điện trường tác dụng (điện di) [45]. Hầu hết các chất keo sinh học có điện tích bề mặt thực âm; do đó, điện thế zeta cao hơn (âm hơn) cho thấy hạt có xu hướng chống lại sự đông tụ hoặc kết tụ với các hạt khác, tương tự- hạt mang điện).
Mặc dù hiệu ứng của ion Hofmeister đối với cấu trúc nước hiện được coi là giới hạn trong một hoặc hai lớp hydrat hóa đầu tiên [42–44], các nghiên cứu quang phổ phân ly hồng ngoại (IRPD) gần đây cho thấy rằng một ion sunfat có thể “sắp xếp” lên đến ca. 36–43 phân tử nước, tương đương với ít nhất ba lớp hydrat hóa [16]. Tuy nhiên, cần lưu ý rằng chưa có dữ liệu IRPD so sánh nào được báo cáo về các anion kosmotropic có ý nghĩa sinh học khác như photphat và cacbonat. Các polysulfat hữu cơ (các phân tử sulfat phức tạp như heparan sulfat, như trong Hình 1) trang trí bên ngoài của gần như tất cả các tế bào trong cơ thể, và chúng rất cần thiết cho chức năng của glycocalyx lót thành đèn trong tất cả các mạch máu [46]. Các tác động có lợi, trong phạm vi dài hơn của các polysulfat hữu cơ như glycosaminoglycans đã sulfat hóa này lên cấu trúc nước sinh học được xem xét dưới đây.
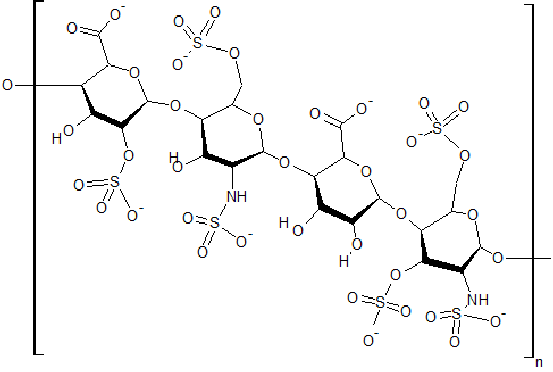
Giống như các ion kosmotropic, các phân tử nhỏ, không chứa ion kỵ nước cũng có thể tạo ra trật tự cục bộ của các phân tử xung quanh. Tuy nhiên, với các chất tan nhỏ không phân cực, sự sắp xếp lại nước cục bộ này làm mất đi đáng kể entropi — với thuật ngữ “entropy” được sử dụng ở đây theo nghĩa nhiệt động lực học cổ điển liên quan đến “rối loạn” hoặc “không có năng lượng cho công việc hữu ích”. Mất entropi bị biến đổi về mặt nhiệt động lực học và do đó làm phát sinh hiệu ứng kỵ nước (khả năng hòa tan thấp của các vi khuẩn ưa nước) ở quy mô dưới ca. 1 nm. Tuy nhiên, các mô phỏng động lực học phân tử với các quả cầu cứng và các tấm graphene chỉ ra rằng các tương tác kỵ nước giữa các bề mặt lớn hơn là entanpi- chứ không phải theo hướng entropi [47,48], trong đó “entanpi” (một thuật ngữ nhiệt động lực học khác) đề cập đến năng lượng nhiệt được truyền trong một hằng số -quá trình áp suất, chẳng hạn như một phản ứng hóa học hoặc loại tương tác giữa các phân tử khác. Hiệu ứng kỵ nước trong các hệ thống sinh học sẽ được thảo luận kỹ hơn dưới đây.
4.2. Nước giữa bề mặt: Tương tác với bề mặt ưa nước và kỵ nước
Trong các hệ thống sinh học, nước lỏng không chỉ tương tác với các chất tan nhỏ mà còn với nhiều bề mặt kỵ nước và lớn hơn, kéo dài hơn, chẳng hạn như bề mặt của protein, axit nucleic, các bào quan khác nhau và màng tế bào. Kết quả của các nghiên cứu về tán xạ neutron không đàn hồi không kết hợp của một số loại tế bào và mô cho thấy rằng ca. 20% –30% tổng số nước (nội bào và ngoại bào) trong các hệ thống này là nước giao diện, tức là nước nằm trong vòng 1–4 nm của các bề mặt này, với nước khối bao gồm 70% –80% còn lại [13]. Không có gì ngạc nhiên khi các nghiên cứu thực nghiệm và tính toán cho thấy những thay đổi khác nhau về đặc tính của nước ở bề mặt kỵ nước và kỵ nước ở cấp độ nano này. Nước giữa bề mặt gần các bề mặt ưa nước như kim cương hydroxyl hóa hoặc silica vô định hình hiển thị độ nhớt lớn hơn từ 2 đến 106 lần so với nước dạng khối, trong khi không thấy sự thay đổi độ nhớt đáng kể của nước gần các bề mặt kỵ nước như silica metyl hóa hoặc kim cương hydro hóa [49,50].
Điều thú vị nhất là, sự tiếp xúc của bề mặt kim cương tinh thể nano hydro hóa kỵ nước với ánh sáng laser 670 nm đã cho ra bằng chứng về sự kích thích liên kết hydro và kết quả là sự giảm mật độ/tăng thể tích trong nước bề mặt, trong khi nước dạng khối về cơ bản là trong suốt đối với bước sóng này [51]. Kết quả này phù hợp với dự đoán của Chandler và cộng sự. Dựa trên các nghiên cứu tính toán chỉ ra rằng, nước ở gần các bề mặt kỵ nước mở rộng (> khoảng 1 nm) cho thấy ít liên kết hydro hơn và hoạt động giống nước gần bề mặt phân cách lỏng-hơi hơn là nước khối [47,52–57]. Ý nghĩa đầy đủ của quan sát này và lý thuyết Lum-Chandler-Weeks đối với luận điểm trung tâm của chúng tôi về căn nguyên bệnh do EIWS gây ra sẽ được thảo luận sau trong bài viết này.
Trong lịch sử, sự tương tác của nước với các phân tử sinh học lớn, đặc biệt là các miền không phân cực của chúng, chủ yếu được xem xét theo quan điểm của đại phân tử và được coi là hiệu ứng kỵ nước. Rezus và Bakker mô tả nó là xu hướng của các nhóm apolar liên kết trong dung dịch nước, do đó giảm thiểu tổng bề mặt kỵ nước tiếp xúc với nước [58]. Trước đó, vào năm 2004, Despa, Fernandez và Berry đã chỉ ra rằng nước bị hạn chế bởi các thủy ngân hoa trải qua một hiệu ứng động lực thư viện làm giảm độ nhạy điện môi và tạo ra “dịch chuyển đỏ” của tần số giãn ra trong vỏ thủy hóa [59]. Sau đó, vào năm 2006, Despa đã mô tả cách nước trong các mô và tế bào bị hạn chế và chịu các tác động cấu trúc không có trong phần lớn của nó. Despa nói thêm rằng hiệu ứng cấu trúc của nước hạn chế trong các mô cũng là một nguồn của trường phân cực góp phần vào sự tương tác hiệu quả giữa các đại phân tử. Hành vi khác nhau của các phân tử nước tại các vị trí ưa nước so với các vị trí kỵ nước được cho là thúc đẩy tính dị hướng của vỏ hydrat hóa của protein. Theo Despa, tính dị hướng của vỏ hydrat hóa là điều cần thiết cho chức năng của enzym [60].
Chưa có sự đồng thuận nhất định nào về cấu trúc của nước gần các bề mặt kỵ nước của các phân tử sinh học. Trong khi cấu trúc “giống clathrate” (mạng lưới, đôi khi là các tấm xếp lớp, hoặc dạng lồng) của quá trình hydrat hóa kỵ nước đã được đề xuất, nghiên cứu và có vẻ hợp lý, một số nghiên cứu cho thấy các hiệu ứng tái cấu trúc tinh vi hơn liên quan đến lớp hydrat hóa thứ hai [61–64] . Chủ đề về cấu trúc hydrat hóa kỵ nước được thảo luận trong một bài báo đánh giá xuất sắc về nước trong sinh học tế bào do Ball viết năm 2008 [65]. Keutsch và Saykally đã trình bày một tổng hợp của quang phổ đường hầm-quay-vòng-rung-quay bằng la-de terahertz và phổ tia la-de giữa tia hồng ngoại của một số đám nano nhỏ của nước, bao gồm một lục phân tuần hoàn của nước có cấu trúc lồng có chất lượng giống như clathrate nhất định đối với vẻ bề ngoài của nó [66] . Các mô phỏng động lực học phân tử đã chỉ ra rằng các pentamer tuần hoàn là cấu trúc liên kết chiếm ưu thế trong nước lỏng. Csajka và Chandler đã phát hiện ra rằng các dạng giống pentamer rất quan trọng trong quá trình hòa tan các chất hòa tan kỵ nước và trong cấu trúc của hydrat clathrat [67]. Đáng chú ý, cấu trúc ổn định nhất của hexamer nước được xác định trong pha khí giống với đơn vị cơ bản trong nước đá [66]. Năm 1995, Xantheas đã báo cáo các nghiên cứu đầu tiên về các cụm nước tuần hoàn (H2O) n, với n = 1–6 [68]. Năm 2000, Nauta và Miller đã xác định được một hexamer nước tuần hoàn trong helium lỏng gần giống với sáu dạng vòng ghi nhớ được tìm thấy trong các dạng băng kết tinh của nước [69].
Theo Perez và các cộng sự, theo lý thuyết, cụm nước được dự đoán là cụm nước nhỏ nhất có mạng lưới liên kết hydro ba chiều là cấu trúc năng lượng tối thiểu của nó. Công trình thí nghiệm trước đây đã cung cấp bằng chứng về các đồng phân dạng lồng, dạng sách và vòng tuần hoàn của nước hexameric. Sử dụng quang phổ quay băng thông rộng trong sự mở rộng siêu âm theo xung, nhóm này xác định rõ ràng cả ba đồng phân cùng tồn tại. Cái lồng được coi là cấu trúc năng lượng tối thiểu. Phổ quay phù hợp với cấu trúc heptamer và nonamer cũng được báo cáo [70].
Bằng chứng về sự hình thành lớp nano nước gần bề mặt lipid gần đây đã được báo cáo bởi Piatkowski và cộng sự. [71]. Bằng cách sử dụng chuyển động năng lượng dao động cực nhanh, họ phát hiện ra rằng nước hydrat hóa màng 1,2-dioleoyl-sn-glycero-3-phosphocholine (DOPC) tạo thành các đám nano ở mức độ hydrat hóa thấp với khoảng cách giữa các phân tử trung bình là 3,4 Å. Xem hình 2 bên dưới để biết vị trí tương đối giả định của các phân tử nước. Trong khi mật độ của các cụm nano nước tăng lên khi mức độ hydrat hóa ngày càng tăng, thì khoảng cách trung bình giữa các phân tử lại không [71].
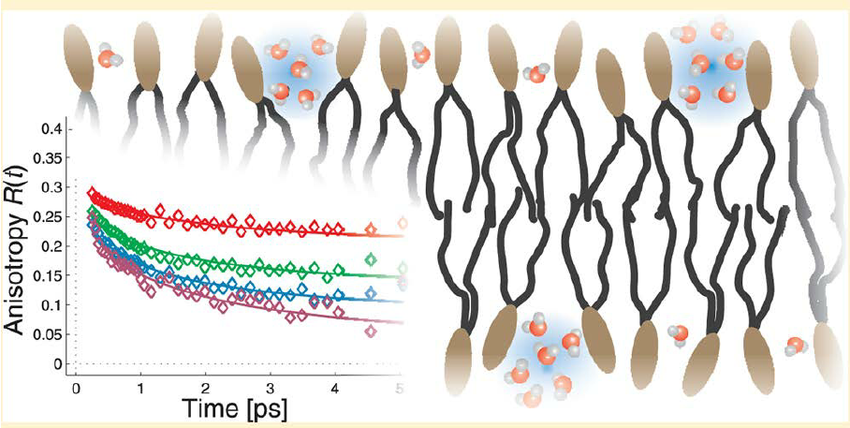
Giống như các nhóm phân cực của màng lipid, polysulfat sinh học cũng có một bề mặt ưa nước mở rộng tương tác với nước. Thậm chí còn có một số bằng chứng về ảnh hưởng trong phạm vi dài hơn của polysulfat sinh học đối với cấu trúc nước. Các phát hiện đặc biệt liên quan đến cấu trúc của nước ngoại bào gần bề mặt màng tế bào, được trang trí rất nhiều bằng các HSPG giàu sulfat được sắp xếp trong các cấu trúc lồi gọi là glycocalyces. Quan sát mô hình khuếch tán của thuốc nhuộm được thêm vào các mạch máu sống cho thấy một lớp nước giống như gel, không thể thấm qua bên trong, thành mao mạch giàu HSPG [72,73]. Kết quả này gợi nhớ đến các nghiên cứu trong ống nghiệm do Pollack et al. về hành vi của nước gần bề mặt ưa nước, tích điện cao của ống và tấm làm bằng Nafion, một chất fluoropolymer sulfo hóa [74–76]. Lớp nước bề mặt nhớt, kéo dài tới 200-300 µm từ bề mặt Nafion và hầu như không chứa ion hoặc chất hòa tan khác, được Pollack mô tả là “vùng loại trừ” (EZ), hoặc pha thứ 4 của nước. Độ dày của EZ có thể tăng lên từ hai đến bốn khi tiếp xúc với bức xạ IR [77]. Liệu những kết quả in vitro thực nghiệm này có liên quan đến sinh lý học in vivo hay không vẫn còn được xác định.
Các thuộc tính của các đặc khu kinh tế được Pollack và các đồng nghiệp mô tả trùng lặp ở một mức độ nào đó với các đặc tính của “miền liên kết” (CD) do del Giudice và cộng sự đề xuất. dựa trên các tính toán lý thuyết trường lượng tử [78]. Đĩa CD nước là một ca. 0,1 µm thu ca. một triệu phân tử nước lỏng dao động điều hòa với trường điện từ tự bẫy ở một số tần số xác định rõ. Lo và đồng nghiệp [79]. Các EZ có thể được coi là tập hợp các đĩa CD tầm xa hơn, và một số nhà nghiên cứu sử dụng hai thuật ngữ này thay thế cho nhau [78]. Các CD / EZ này tạo ra một thế điện âm tới -150 mV so với nước lỏng “bình thường” liền kề và nồng độ proton tương ứng tại mặt phân cách với nước “bình thường”. Tính chất vật lý chi tiết của loại nước này, như được tiết lộ bởi các nghiên cứu trong ống nghiệm của Pollack và cộng sự, chỉ mới được làm sáng tỏ gần đây và việc điều tra về ý nghĩa lâm sàng tiềm năng đã được đảm bảo.
4.3. Tương tác với Điện trường và Từ trường
Trong phần này, chúng tôi khảo sát các tài liệu gần đây liên quan đến tác động của điện trường và từ trường đối với cấu trúc và đặc tính của nước giao thoa. Chúng tôi cũng sẽ xem xét bằng chứng chỉ ra hệ thống tín hiệu Ca2 + là mục tiêu chính của tế bào của từ trường, vì điều này có ý nghĩa quan trọng đối với việc hấp thụ xenobiotics độc hại, bao gồm cả các yếu tố gây căng thẳng nước qua mặt như Al3 +, vào tế bào.
Các bằng chứng sẵn có chỉ ra các tác động khác nhau của điện trường và từ trường đối với cấu trúc nước. Năm 2008, Rai et al. báo cáo kết quả tính toán lý thuyết hàm mật độ chỉ ra rằng điện trường áp dụng “mở ra” các cụm nước dạng vòng hoặc vòng để tạo thành cấu trúc tuyến tính, phân nhánh hoặc dạng lưới bằng cách làm cho các monome nước lưỡng cực thẳng hàng dọc theo trục trường. Nói chung, số lượng liên kết hydro trong một cụm giảm khi cường độ điện trường tăng lên [80]. Năm 2011, Acosta-Gutierrez et al. thực hiện các nghiên cứu tính toán bổ sung về các đặc tính vật lý của các cụm nước nhỏ trong điện trường thấp và trung bình. Ở cường độ điện trường thấp, các liên kết hydro định hướng các lưỡng cực vĩnh cửu của nước dọc theo trường, trong khi cường độ trường lớn hơn gây ra sự tái tổ chức cấu trúc rộng rãi hơn, bao gồm việc phá vỡ liên kết hydro khi cụm kéo dài dọc theo hướng trường, với “các cụm lớn hơn (N> 10) thường hình thành các cấu trúc xoắn ốc ”[81].
Ngược lại với các nghiên cứu tính toán cho thấy rằng điện trường bên ngoài phá vỡ các cụm nước nhỏ và khiến các monome nước xếp thành hàng theo hướng của trường, kết quả mô phỏng động lực học phân tử của Chang và Weng ngụ ý rằng từ trường bên ngoài làm tăng độ ổn định và hydro độ bền liên kết của các cụm nước siêu phân tử trong khi làm giảm sự tự khuếch tán của các phân tử nước riêng lẻ [82]. Hơn nữa, dữ liệu thực nghiệm do Pang et al. về tác động của từ trường bên ngoài lên các đặc tính của nước [83–86] ủng hộ giả thuyết trước đó của Pang rằng những trường như vậy thúc đẩy sự hình thành của cả chuỗi thẳng và chuỗi khép kín của các phân tử nước liên kết hydro [87]. Áp dụng từ trường nằm trong khoảng từ 2000 đến 4400 G (0,20–0,44 T), Pang và Deng nhận thấy rằng sự hấp thụ tia hồng ngoại và tia cực tím, tán xạ Raman và nhiễu xạ tia X của nước nhiễm từ đã thay đổi đáng kể so với sự hấp thụ của nước không tiếp xúc: tia hồng ngoại (IR ) cường độ đỉnh tăng lên, tần số của một số đỉnh thay đổi, và một số đỉnh mới xuất hiện sau khi nước được từ hóa [83,84]. Các hiệu ứng từ trễ đáng kể đã được quan sát thấy trong phổ hấp thụ IR của nước nhiễm từ khi nhiệt độ được tăng lên và sau đó giảm trong phạm vi từ 25 ° C đến 70 ° C. Điều quan trọng là, nước nhiễm từ thể hiện góc tiếp xúc thấp hơn (tính kỵ nước thấp hơn hoặc tăng khả năng hòa tan các bề mặt kỵ nước) so với nước không nhiễm từ với các bề mặt đồng, graphit và muscovite. Đối với mỗi bề mặt, chênh lệch góc tiếp xúc giữa nước nhiễm từ và nước không nhiễm từ là nhỏ, theo thứ tự từ 0,4 đến 1,4, nhưng vẫn nằm ngoài phạm vi sai số thực nghiệm của thiết bị. Từ trường bên ngoài làm tăng chiết suất, hằng số điện môi và độ dẫn điện của nước trong khi giảm độ nhớt của nó [84]. Thời gian từ hóa càng dài, độ nhớt của nước bị nhiễm từ càng giảm, cho đến khi đạt mức tối thiểu.
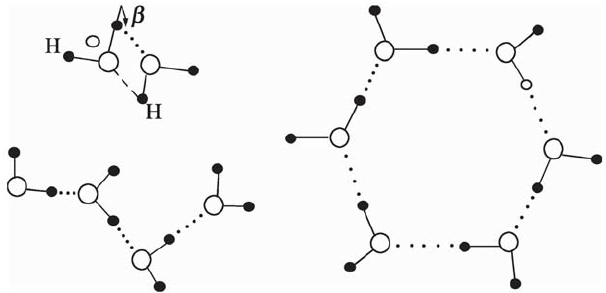
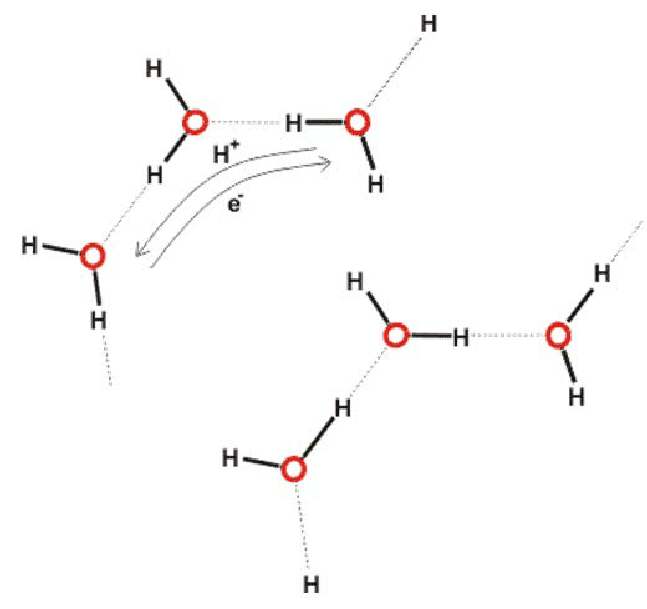
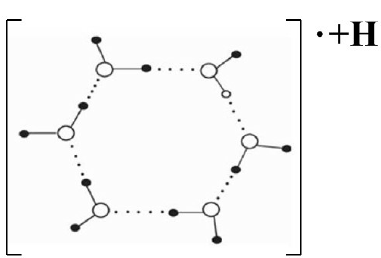
Như đã đề cập ở trên, kết quả của những nghiên cứu thực nghiệm này về tác động của từ trường đối với tính chất của nước [83–86] phù hợp với đề xuất trước đó của Pang rằng sự tiếp xúc của nước với từ trường tạo điều kiện hình thành các cụm nước liên kết hydro tuyến tính và khép kín, sau này trong số đó có thể trở thành các phần tử dòng điện vòng hoặc “dòng điện phân tử” có từ tính do độ dẫn proton của chúng dưới tác dụng của lực Lorentz [87]. Điều này cho phép tương tác từ của các phần tử “dòng điện phân tử” này với nhau hoặc với từ trường tác dụng bên ngoài để thay đổi sự phân bố và tính năng của các phân tử nước và “từ hóa của nước” [83]. −Ví dụ về các chuỗi liên kết hydro tuyến tính (mở) và tròn (kín) được đề xuất của các phân tử nước được thể hiện trong Hình 3.
Như đã nói ở trên, kết quả của thí nghiệm này là nghiên cứu về tác dụng của từ trường đối với nướccác tính chất [83–86] nhất quán với đề xuất trước đó của Pang rằng sự tiếp xúc của nước với từ tínhlĩnh vực tạo điều kiện cho hình thứckhái niệm về các cụm nước liên kết hydro tuyến tính và khép kín , cụm nước sau có thểtrở thành dòng điện vòng hoặc “dòng điện phân tửphần tử nt ”có từ tính do họ độ dẫn của proton dưới tác dụng của lực Lorentz [87]. Th là cho phép mtương tác từ tính của những “dòng điện phân tử” nàymối quan hệ với nhau hoặc với bên ngoài từ tính áp dụng trường để thay đổi sự phân bố và tính năng của các phân tử wa ter và “ độ phân cực từ của nước” [83].-Ví dụ về các chuỗi liên kết hydro thẳng (mở) và tròn (kín) được đề xuất của nướccác phân tử được thể hiện trong Hình 3.
Các cường độ từ trường 0,20–0,44 T được Pang và Deng sử dụng cao hơn vài bậc độ lớn so với cường độ của trường địa từ trên bề mặt trái đất (khoảng 50 µT) và thậm chí cao hơn ca. 10-10–10-15 giá trị T đo được cho các cơ quan của người [3,4]; do đó, sự liên quan của các nghiên cứu của họ đối với nước trong các hệ thống sinh học có thể được đặt ra một cách hợp pháp. Tuy nhiên, một cơ chế bổ sung của từ hóa nước, được trình bày bởi Mohri [88,89], dựa trên các nghiên cứu thực nghiệm liên quan đến từ trường xung 6 Hz, 10 µT liên quan đến mặt sinh lý hơn. Giả thuyết của Mohri liên quan đến giả định về sự cộng hưởng cyclotron của các cụm nước được proton hóa (H3O + (H2O) n).
Cộng hưởng Cyclotron đề cập đến hiện tượng truyền năng lượng cho một hạt tích điện đang chuyển động tròn đều, bình thường theo hướng của từ trường tác dụng, như là một biểu hiện của lực Lorentz; cái gọi là “tần số cộng hưởng cyclotron” của chuyển động tròn này phụ thuộc vào điện tích và khối lượng của hạt cũng như cường độ của từ trường. Theo Mohri, hiệu ứng cộng hưởng cyclotron này kích hoạt quá trình vận chuyển proton trong nước theo từ trường địa từ, một hiệu ứng được mô tả là “từ tính protonics” [89]. Sự hình thành một chuỗi các cụm nước cộng hưởng như vậy có thể làm tăng khả năng dẫn proton. Giả thuyết này phù hợp với sự giảm điện trở suất của nước nhiễm từ được Mohri báo cáo trong các nghiên cứu được tiến hành với từ trường xung, yếu được mô tả ở trên [89].
Ngoài việc ảnh hưởng đến các đặc tính của nước giao diện, từ trường cũng có thể gây ra những thay đổi trong nhiều hệ thống tín hiệu Ca2 + sinh học. Năm 2002, Mohri nhận thấy hoạt động miễn dịch thực bào tăng cường và nồng độ Ca2 + nội bào tăng cao trong bạch cầu trung tính tiếp xúc với dung dịch muối đệm phosphat (PBS) đã chịu tác động của từ trường AC tần số cực thấp milliGauss (mg ULF-AC) trước khi tiếp xúc với bạch cầu trung tính với nó [90]. Trong một nghiên cứu tiếp theo, Mohri đã báo cáo một phương pháp đáng tin cậy để làm giảm điện trở suất của nước tinh khiết cao bằng cách áp dụng một từ trường nhỏ vài miliGauss với biên độ và tần số cộng hưởng cyclotron kép là 7,0 Hz và 8,4 Hz để kích thích các cụm phân tử thủy lực hexameric và pentameric tương ứng. [88].
Năm 2005, Fukushima và cộng sự. đã báo cáo một phát hiện phi thường khác: nước tinh khiết tiếp xúc với từ trường AC 10 mG, tần số cực thấp (6 Hz) (được tạo ra bởi cuộn dây Helmholtz dưới ánh sáng nhìn thấy) đã kích thích đom đóm phát quang luciferin-luciferase và gây ra sự nâng cao Ca2 + nội bào của buồng trứng chuột hamster Trung Quốc ( CHO) các tế bào trong điều kiện không có ATP [91] đưa ra giả thuyết rằng việc tiếp xúc với từ trường sẽ làm tăng hoạt động truyền tín hiệu mà không đánh thuế các nguồn năng lượng bình thường. Do đó, sự phát quang do luciferase xúc tác của luciferin, vốn thường yêu cầu ATP trong nước chưa được xử lý, xảy ra mà không cần thêm ATP nào trong nước đã được xử lý bằng từ trường và ánh sáng. Thật vậy, hoạt động phát quang của phức hợp luciferin-luciferase trong nước tiếp xúc với từ trường và ánh sáng cao hơn nhiều lần so với hoạt động phát quang trong điều kiện được che chắn ánh sáng. Cần lưu ý rằng các thí nghiệm này được tiến hành ở 40 ° C, gần với nhiệt độ cơ thể người bình thường là 37 ° C và gần nhiệt độ tối ưu cho hầu hết các phản ứng enzym. Tần số 6 Hz của từ trường được đặt vào tương ứng với tần số cộng hưởng cyclotron của cụm nước hexameric proton H3O + (H2O) 5 dưới tác động của trường địa từ (khoảng 500 mG) và với tần số sóng alpha của não [ 88,91]. Các tác giả suy đoán rằng năng lượng từ trường áp dụng cho nước tinh khiết được lưu trữ trong một cụm nước có cộng hưởng liên kết hydro ổn định và được chuyển đến phức hợp luciferin-luciferase, kết quả là sự hình thành oxy-luciferin và phát quang khi không có ATP [91].
Mặc dù kết quả của Fukushima và các đồng nghiệp [91] có vẻ đáng ngạc nhiên, công trình gần đây chỉ ra khả năng của ánh sáng mặt trời entropy thấp trong việc truyền tải một lượng lớn trật tự tầm xa cũng như nước mặt [92] cung cấp một lộ trình hợp lý mà CD nước có thể cung cấp. năng lượng xúc tác cho các phản ứng hóa học không chỉ ở các enzym mà còn thực sự gần nhiều bề mặt kỵ nước hoặc ưa nước [93,94], cũng như cho sự khuếch tán thực tế của các enzym qua dung dịch nước số lượng lớn đến các khu vực có nồng độ cơ chất cục bộ cao [95-97].
Kết quả thu được của Fukushima và đồng nghiệp [91] phù hợp với kết quả của Gartzke và cộng sự. (2002), người đã chỉ ra hệ thống tín hiệu Ca2 + là mục tiêu chính của từ trường tế bào. Cụ thể, bó sợi actin dẫn ion trong vi nhung mao đã được đề xuất làm mục tiêu của tế bào cho từ trường. Mục tiêu này kết hợp sự liên quan sinh lý đối với tín hiệu Ca2 + với các đặc tính điện bất thường có khả năng giải thích ảnh hưởng của từ trường năng lượng thấp đối với các hệ thống sinh học [98]. Mục tiêu này trước đây đã được chứng minh là thể hiện sự dẫn truyền cation dạng cáp, phi tuyến qua các mảng các đám mây ion ngưng tụ. Cộng hưởng ngẫu nhiên và / hoặc giả thuyết động cơ Brown đã được sử dụng để giải thích sự tương tác của các đám mây ion với các trường điện từ được ứng dụng định kỳ dẫn đến việc bơm cation qua một dãy các rào cản tiềm năng bên trong các polyelectrolytes [98]. Cơ chế tương tác được đề xuất phù hợp với độ nhạy cực độ đã được công nhận đối với kích thích bởi năng lượng trường rất thấp trong các cửa sổ biên độ và tần số cụ thể. Do đó, thay vì đóng vai trò gây nhiễu, bản thân “nhiễu” nhiệt đã trở thành một thành phần tín hiệu thiết yếu và cần thiết. Quá trình truyền cation vi mô bởi các bó F-actin được che chắn bởi màng lipid khuếch đại các tín hiệu mạch lạc trên quá trình truyền cation và giảm nhiễu ngẫu nhiên (nhiệt). Các tín hiệu kết hợp yếu được cho là được khuếch đại bởi nhiễu nhiệt thông qua cộng hưởng ngẫu nhiên xảy ra khi áp dụng trường năng lượng rất thấp được áp dụng định kỳ, dẫn đến vận chuyển cation một chiều dọc theo các bó F-actin.
Một hàm ý quan trọng của hệ thống hóa được đề xuất này là tác động hiệp đồng của từ trường đối với việc hấp thụ xenobiotics vào tế bào. Các hợp chất độc hại có thể xâm nhập vào tế bào dễ dàng hơn dưới tác động của trường điện từ, kích hoạt con đường tín hiệu Ca2 +. Lange chỉ ra rằng việc duy trì các bề mặt vi mô còn nguyên vẹn là điều cần thiết trong việc cung cấp chức năng rào cản tự nhiên của các tế bào biểu mô [99]. Bất kỳ sự vô tổ chức nào của hình thái bề mặt vi khuẩn cũng được chứng minh là có thể đẩy nhanh sự xâm nhập của xenobiotics ion và ưa béo vào tế bào chất. Điểm này sẽ được thảo luận kỹ hơn trong Phần 5 và 6 dưới đây khi chúng ta xem xét các tác động bất lợi của cation nhôm và các tác nhân gây căng thẳng nước giao diện ngoại sinh khác đối với các hệ thống sinh học.
4.4. Các thuộc tính tạo sự sống của nước ở giai đoạn giữa các pha
Chúng tôi đề xuất rằng các hệ thống chính mà nước giao thoa có cấu trúc thúc đẩy các quá trình sinh học tạo điều kiện cho sự sống bao gồm:
(A) Thúc đẩy tính dẫn điện tại các bề mặt sinh học, do đó tạo điều kiện thuận lợi cho quá trình trao đổi chất và sự khác biệt điện thế được duy trì bởi các bào quan nội bào;
(B) Hấp thụ, lưu trữ và phát ra năng lượng điện từ, cho phép lưu trữ và truyền năng lượng và thông tin;
(C) Khắc phục kT hoặc vấn đề “khuếch tán nhiệt”; và
(D) Giải quyết vấn đề đông đúc nội bào và tự lắp ráp phân tử bằng phương pháp điều hòa (tính thuận tay của các phân tử) và từ hóa.
Những tương tác này sẽ được thảo luận dưới đây, cùng với dữ liệu hỗ trợ.
4.4.4.1. Thúc đẩy tính dẫn điện ở các giao diện sinh học
Các tổ hợp phân tử nano của CD nước ở pha nước có thể cung cấp một khoảng mở rộng, tầm xa, giàn giáo cho sự chuyển giao nguyên tử và điện kế trên quy mô trung mô, siêu phân tử, hỗ trợ quá trình chuyển hóa năng lượng in vivo. Chúng tôi đã đề cập trước đây về vai trò của HSPG bên ngoài trong việc kết nối bộ xương tế bào với màng sinh chất. Bộ xương tế bào cũng đóng một vai trò trung tâm trong vận chuyển lipid dựa trên caveolin giữa bộ máy Golgi và màng sinh chất [100]. Chúng tôi giả thuyết rằng bộ xương tế bào cũng tạo điều kiện thuận lợi cho việc vận chuyển cả electron và proton, tận dụng các CD nước để tạo ra từ trường thúc đẩy dòng proton và electron, do đó duy trì gradient điện thế màng tế bào. Vận chuyển ion tương tự đến và đi từ các bào quan trong tế bào chất như ti thể (phải duy trì độ pH cơ bản cao) và lysosome (phải duy trì độ pH có tính axit cao) cũng có thể được duy trì bởi bộ xương tế bào. Bộ xương actin đã được chứng minh là có liên kết không thể tách rời với cả lysosome [101] và ty thể [102]. Nếu các bào quan này không thể duy trì giá trị pH cực đoan của chúng, chúng sẽ không hoạt động và tế bào sẽ bị vô hiệu hóa.
Hình 3 ở trên mô tả một số đám nano nước có thể có khả năng thúc đẩy tính dẫn của proton [87]. Ba cách sắp xếp cụm nước được đề xuất bổ sung để tăng cường chuyển giao proton được thể hiện trong Hình 4–7 [103–106]. (
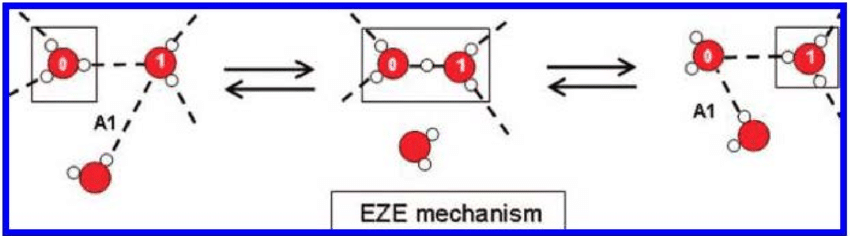
và cộng sự (2008) [105] với sự cho phép của Hiệp hội Hóa học Hoa Kỳ.
Verdel và cộng sự. [106,107] cho rằng sự gia tăng chuyển giao proton suy ra từ các phép đo độ dẫn điện cho hiện tượng “autothixotropic” (hành vi giống như gel yếu) của nước, được cho là phát triển tự nhiên theo thời gian, nơi các ion và bề mặt ưa nước dường như đóng một vai trò quan trọng. Voth và cộng sự. [105,108,109] đã chỉ ra rằng các nhóm sulfonat trong fluoropolymer Nafion sulfonat hóa ảnh hưởng đến quá trình solvat hóa proton dư thừa, cũng như cấu trúc hydrat hóa proton, bằng cách ổn định cấu trúc giống Zundel (H5O2 +) hơn trong lớp vỏ solvat hóa đầu tiên của chúng [110]. Các nhóm sulfonat cũng được phát hiện có ảnh hưởng đến hướng nhảy của proton. Những phát hiện này cho thấy biosulfat hoạt động như thế nào trong cơ thể sống.
Các nghiên cứu với Nafion, được sử dụng trong pin nhiên liệu dựa trên màng trao đổi proton [108,109,111], và với ống nano cacbon (CNTs) có chức năng với các nhóm CF3SO3H [112], đã cung cấp thêm thông tin chi tiết. Ở hàm lượng nước thấp, các chuỗi bên sunfonat hóa của Nafion hình thành các vùng ưa nước cô lập. Khi hàm lượng nước tăng lên, các miền này mở rộng và cuối cùng hình thành các kênh nước trải dài có khả năng truyền proton một cách hiệu quả. Có khả năng là các tế bào nhân thực sử dụng một hệ thống như vậy để vận chuyển proton hiệu quả. Trong các nghiên cứu động lực học phân tử ab ban đầu với CNT được lưu huỳnh hóa bằng fluorosunfat, việc giảm khoảng cách giữa các nhóm sulfonat làm tăng sự phân ly proton và tương tác giữa các phân tử nước. Khi khoảng cách sulfonat-sulfonat tăng lên, khả năng kết nối giữa các phân tử nước giảm xuống do chúng hình thành nhiều cụm cô lập xung quanh các nhóm sulfonat. Khoảng cách và hình học sulfonat-sulfonat là những yếu tố chi phối nhiều nhất trong sự phân ly proton; tuy nhiên, môi trường kỵ nước và giam giữ kích thước nano trở nên quan trọng hơn khi khoảng cách giữa các nhóm sulfonat tăng lên [112].
Martin Chaplin, một chuyên gia ưu việt về cấu trúc và tính chất của nước, gần đây đã lập luận rằng cả sự phân chia proton và electron đều tạo nên trạng thái bình thường của mạng lưới phân tử nước lỏng, như được minh họa bằng sơ đồ trong Hình 6 dưới đây [113,114]. Do đó, nếu ông ấy đúng, thì độ dẫn điện của electron (cũng như proton) được tăng cường trong các cụm CD nước. Czerlinski và Ypma đề xuất rằng các điện tử di chuyển theo thống kê trong các miền điện động như một lưỡng cực, bắt đầu hành vi tương tự trong các miền khác bằng cộng hưởng [115,116]. Khi mạng lưới nước tiếp xúc với bức xạ ion hóa, cấu trúc được thay đổi để tạo độ linh động cho cả proton và gốc hydroxyl [117].
Nhà vật lý lý thuyết, Herbert Frölich, ban đầu đề xuất vào năm 1968 rằng dao động điện cực kết hợp và tạo ra trường điện từ đóng vai trò quan trọng trong tế bào sống, và sự rối loạn của chúng xảy ra trong tế bào ung thư [118,119]. Hỗ trợ thử nghiệm cho các ý tưởng của Frölich tiếp tục được tích lũy. Năm 2013, Pokorný et al. đã xem xét các tài liệu lý sinh hiện hành liên quan đến sự biến đổi ung thư [120], trong đó các phép đo được thực hiện trên tế bào sống đã tiết lộ dao động điện và điện từ, bao gồm cả lực điện di của điện trường dao động tế bào. Lực hút của các hạt điện môi phụ thuộc vào độ cho phép của chúng [121]. Chúng tôi giới thiệu người đọc đến [120] để biết các mô tả về nghiên cứu thực nghiệm và lý thuyết về hoạt động điện từ của tế bào, mà ngày nay, chúng chỉ ra các vi ống là nguồn tương tác điện từ chính. Bằng chứng cho vai trò chính của sự phá vỡ bộ xương tế bào do EIWS gây ra trong việc gây ung thư được thảo luận trong Phần 6.1 dưới đây.
Một lộ trình bổ sung để tăng cường độ dẫn điện trong các hệ thống sinh học có thể là sự phân tách gốc ion chuyển các đám nano nước [122] trung bì thành chất siêu dẫn. Là mesomeric cho phép phân định vị trí của các proton (làm cho các đám nano này là nguyên tố) cũng như các điện tử gốc tự do (làm cho chúng cũng là điện động). Các tính chất như vậy cho phép xúc tác các phản ứng oxy hóa-khử, sự lan truyền của dòng điện và tạo ra từ trường. Các hệ thống Mesomeric, cùng với các cụm nước ổn định khác, về mặt lý thuyết cũng có thể đóng vai trò là phương tiện lưu trữ năng lượng bức xạ sự cố dưới dạng tổn thất entropi và phân tách điện tích, như giả thuyết của Chai, Yoo và Pollack vào năm 2009 [76]. Hình 7 (bên dưới) minh họa một bipolaron theo chu kỳ giả định ― một tập hợp điện kế và nguyên tố của nước có cấu trúc. Một phức hợp như vậy có thể hỗ trợ trong việc duy trì điện thế màng và cho phép dẫn truyền tế bào xương. Các hexamers tuần hoàn ổn định của nước đã được Saykally [66], Pang [84–87] và Mitsui [123] nghiên cứu về mặt phổ và lý thuyết. Chuyển động của điện tử trong các miền kết hợp mở rộng này dường như giống với chuyển động của điện tử tự do trong kim loại hoặc thậm chí chất siêu dẫn [115,124–126]. Các mô hình khác để bắt điện tử trong nước ― ví dụ, các điện tử trong các hốc nước giống quỹ đạo p ― đã được đề xuất và xác minh bằng thực nghiệm [127].
.
Dòng điện phụ thuộc vào sự có mặt của nước đã được phát hiện có liên quan đến cellulose [128], protein [129,130], vi ống [131] và DNA [132,133]. Năm 1987, Careri và cộng sự. đã chứng minh khả năng dẫn proton dòng điện một chiều (DC) của bột lysozyme đối với các mức độ hydrat hóa khác nhau [134,135] và gợi ý rằng sự dẫn truyền proton do hydrat hóa và hoạt động của enzym tương ứng với sự hình thành mạng lưới liên kết của các phân tử nước được hấp thụ trên bề mặt của đại phân tử. Các nghiên cứu mô phỏng trên máy tính được báo cáo vào năm 2006 cho thấy rằng sự thấm nước hydrat hóa trên bề mặt DNA thúc đẩy quá trình chuyển đổi đa hình và độ dẫn DNA [136]. Năm 2012, Sontz et al. đề xuất một cơ chế trung gian vận chuyển điện tích bằng DNA duplex [133]. Các dòng điện này có phụ thuộc vào sự hiện diện của các cụm phân tử nano của đĩa CD nước không? Các tài liệu nghiên cứu cho thấy rằng chúng là như vậy. Czerlinski và Ypma đã cung cấp phần lớn sự hỗ trợ về mặt lý thuyết cho sự dẫn điện (độ dẫn điện tử) của các đĩa CD nước phân tử nano [115,116,137,138]. Với hiệu ứng Josephson trong vật lý và thực tế là các cặp bazơ chồng lên nhau của chuỗi xoắn kép có chất lượng kim loại nhất định, gần giống như các tấm graphit [126,133], không có gì ngạc nhiên khi DNA được liên kết với dòng điện trong thực nghiệm.
Chúng tôi đề xuất rằng các cụm phân tử nano động học của đĩa CD nước đại diện cho các động cơ nano tiêu thụ entropy [139–143] cấu trúc, bẫy, truyền và dẫn năng lượng để tạo ra những thay đổi về cấu trúc trong cả DNA và protein. Khi đó, các cụm nano của nước và DNA được từ hóa có thể hoạt động phối hợp để tạo ra một giàn giáo siêu phân tử hoạt động để truyền cả năng lượng và thông tin trong khoảng cách dài. Bằng chứng thực nghiệm đã được trích dẫn cho thấy rằng ứng suất nước giữa các bề mặt (IWS) cung cấp cơ sở siêu phân tử cho cả sự hình thành và ổn định của các vòng DNA tròn [144], microDNA [145], DNA không phải B [146] và Z-DNA [147]. IWS và các cụm nano của nước từ hóa cũng cung cấp cơ sở siêu phân tử để điều chỉnh sự ổn định cấu trúc DNA về cả sức khỏe, ví dụ, sự phân chia tế bào bình thường và bệnh tật, ví dụ, bệnh ung thư. Chủ đề này được khám phá sâu hơn trong Phần 6 dưới đây.
4.4.2. Hấp thụ, lưu trữ và phát ra năng lượng điện từ
Ngoài khả năng tăng cường độ dẫn điện, nghiên cứu liên quan và lý thuyết âm thanh cho thấy đĩa CD nước có thể hấp thụ và phát ra năng lượng điện từ, do đó lưu trữ và truyền cả thông tin và năng lượng [148–150]. Nước EZ hấp thụ ánh sáng ở bước sóng 270 nm và phát huỳnh quang khi bị kích thích ở bước sóng này [151]. Một phần dựa trên ứng dụng lý thuyết trường điện động lượng tử của Preparata [152–154], Marchettini, Del Giudice, Fuchs, Vitiello, và Voeikov đã đề xuất vào năm 2010 rằng đĩa CD nước cung cấp một “đống oxy hóa khử” gồm “các điện tử gần như tự do” [78,155] . Năm 1998, Voeikov và Naletov mô tả sự phát xạ photon yếu của các phản ứng hóa học không tuyến tính của axit amin và đường trong dung dịch nước mà họ đề xuất cung cấp bằng chứng cho các phản ứng dây chuyền tự tổ chức với sự phân nhánh chậm [149]. Năm 1999, Kobayashi báo cáo sự phát xạ photon siêu yếu tự phát từ não chuột có liên quan đến chuyển hóa năng lượng não và stress oxy hóa [156]. Năm 2004, Curtis và Hurtak [157] đã đề xuất rằng các quá trình biophotonic ở người có thể đại diện cho cách ánh sáng lý sinh tương tác với quá trình tự tổ chức thông tin của con người có thể đạt được bằng phương tiện trao đổi chất sinh học hoặc giao tiếp thần kinh.
Năm 2005, Kim và cộng sự đã chứng minh rằng sự phát xạ photon tự phát từ các mô ung thư tương phản với sự phát xạ của các mô bình thường, và đặc tính phát quang chậm của chúng đã được nghiên cứu [158,159]. Giá trị trung bình của sự phát xạ photon tự phát từ các mô bình thường và mô khối u được đo với sai số tiêu chuẩn lần lượt là 625 ± 419 số đếm / phút / cm2 (n = 6) và 982 ± 513 số đếm / phút / cm2 (n = 14). Giá trị đỉnh của cường độ phát quang chậm từ các mô bình thường và mô ung thư lần lượt là 63 ± 20 đếm / ms (n = 6) và 48 ± 12 đếm / ms (n = 14) [158].
Vào năm 2007, Whissell và Persinger đã chỉ ra rằng sự tiếp xúc trước khi sinh của những con chuột bạch tạng Whistar đang mang thai với từ trường cực kỳ yếu 7 Hz trong phạm vi 1, 5, 10, 50 và 500 nT, gây ra những khiếm khuyết về hành vi ở con cái của chúng và kéo dài đến tuổi trưởng thành. Những thay đổi này được phát hiện là đặc trưng cho dạng sóng và có thể liên quan đến oxit nitric [160]. Sử dụng đồng thời chất ức chế nitric oxide synthase (NOS) n-methylarginine dường như để giảm thiểu các hành vi thiếu hụt do từ trường gây ra, cho thấy vai trò phát triển quan trọng của NO và sự tham gia của NO trong các hiệu ứng từ trường [160]. Liệu những phát hiện này có thể cho thấy cách một trường điện từ bên ngoài điều chỉnh IWS dẫn đến phản ứng protein mở ra (UPR), có lẽ bằng cách tăng tính kỵ nước của nước? Quá trình hoạt hóa NOS yêu cầu liên kết canxi với calmodulin. Như đã nói trước đây, canxi là một mục tiêu tế bào được đề xuất của từ trường. Về nguyên tắc, từ trường có thể làm thay đổi lưu lượng máu trong mạch do tác động của chúng lên eNOS hồng cầu và eNOS nội mô. Nếu tần số cộng hưởng cyclotron ion (ICR) của canxi được gây ra bởi từ trường, hiện tượng này có thể được tổng quát hóa cho một số chức năng lớn hơn, do vai trò đa dạng của canxi trong các con đường tín hiệu sinh học [161].
Năm 2010, Tafur và cộng sự đã đề xuất rằng việc phát hiện ra các photon sinh học, việc sản sinh ra chúng có liên quan đến trạng thái oxy hóa khử của tế bào và tạo ra ROS, đại diện cho một biện pháp oxy hóa khử không xâm lấn có thể hữu ích trong việc thúc đẩy liệu pháp ánh sáng cường độ thấp [162]. Vào năm 2011, Czerlinski đã mô tả các miền nano nước tồn tại lâu dài tạo thành các tập hợp hợp tác chặt chẽ được kiểm soát bởi trường địa từ. Các miền này phát ra từ từ các photon sinh học hoặc thực hiện các công việc sinh hóa cụ thể tại mục tiêu của chúng [115,116].
Vào năm 2012, Pang [83,84,86] đã xác định từ phổ năng lượng rằng các phân tử protein có thể vừa bức xạ vừa hấp thụ các photon sinh học có bước sóng <3 μm và 5–7 μm, phù hợp với sự chuyển đổi mức năng lượng của exciton, và phù hợp với dữ liệu hấp thụ tia hồng ngoại thực nghiệm. Phát hiện của Pang dường như hỗ trợ cho các kết quả thí nghiệm gây tranh cãi của Gerald Pollack vào năm 2006 [77] trong đó các EZ lớn được quan sát thấy ở vùng lân cận của nhiều loại bề mặt, bao gồm hydrogel nhân tạo và tự nhiên, mô sinh học, polyme ưa nước, đơn lớp và ion- hạt trao đổi, cũng như với nhiều loại chất tan. Hơn nữa, nó đã được chứng minh thêm rằng năng lượng bức xạ mở rộng một cách sâu sắc các vùng này theo cách thuận nghịch, phụ thuộc vào bước sóng. Pollack đã viết: “Có vẻ như năng lượng bức xạ sự cố có thể được lưu trữ trong nước dưới dạng mất entropi và phân tách điện tích” [76]. Liệu các kết quả trong ống nghiệm của Pollack có áp dụng cho trạng thái sống, ví dụ: sinh học tế bào hay không vẫn còn được xác định.
4.4.3. Khắc phục vấn đề kT hoặc “Khuếch tán nhiệt”
Theo Ho (2011), “ngưỡng nhiệt” là một sự ngụy biện xuất phát từ giả thiết rằng các sinh vật sống có thể được mô tả dưới dạng nhiệt động lực học cân bằng thông thường; trong khi theo sự nhất trí chung, chúng là những hệ thống mở được tổ chức một cách tỉ mỉ và duy trì rất xa so với trạng thái cân bằng nhiệt động lực học [163]. CD nước có thể cung cấp cơ sở vật lý để khắc phục cả nghịch lý kT và vấn đề đông đúc nội bào [28,29,31,164–172] không? Thuật ngữ yêu cầu kT, trong đó k là hằng số Boltzmann và T là nhiệt độ (độ K), nói chung liên quan đến sự phụ thuộc nhiệt độ của tốc độ phản ứng hóa học và nhu cầu truyền đủ năng lượng cho các phân tử sinh học trong tế bào để đạt được phản ứng như vậy ở nhiệt độ sinh lý. , mà không cần đến sự khuếch tán nhiệt (tức là làm nóng các chất phản ứng).
Thông qua khả năng lưu trữ và khuếch đại năng lượng điện từ, CD nước cung cấp một phương tiện để đạt được các hiệu ứng sinh học với từ trường rất yếu bằng cộng hưởng cyclotron ion (ICR), như đã thấy trong Phần 4.3 ở trên, và bằng các phương tiện không phụ thuộc vào nhiệt độ [78,163,166,167,169,173,174]. ICR chỉ cung cấp một trong những cách khác nhau để giải thích về mặt lý thuyết cho các tương tác quan sát được giữa các trường điện từ tần số thấp yếu và các hệ thống sinh học. Giả thuyết ICR đã được trình bày chi tiết vào năm 2006 bởi A.R. Liboff. từ trường tĩnh và từ trường xoay chiều yếu [167,176,177].
4.4.4. Giải quyết các vấn đề về sự đông đúc trong tế bào và sự tự lắp ráp của các phân tử bằng Phương thức Chirality và Từ hóa
Rõ ràng là pha nước của tế bào chất đông đúc hơn là loãng, và sự khuếch tán và phân chia của các đại phân tử và túi trong tế bào chất bị hạn chế rất nhiều bởi sự cản trở của steric cũng như bởi các tương tác liên kết không mong muốn [170,171,178]. Năm 2001, Aggeli et al. đã trình bày một mô hình cơ học thống kê chung để tự lắp ráp các đơn vị giống hình que bất đối, chẳng hạn như peptit tạo tấm beta, thành các băng xoắn, với nồng độ ngày càng tăng, liên kết thành các dải xoắn (băng kép), các sợi (các ngăn xếp xoắn của ruy-băng), và sợi (các sợi quấn vào nhau) [179]. Kết quả của một nghiên cứu gần đây về hành vi tự lắp ráp của các đồng phân của tripeptit kỵ nước leu-phe-phe cho thấy rằng các protein bao gồm các axit amin đồng phân có thể sẽ lắp ráp và đóng gói hiệu quả hơn các protein chứa cả axit amin D- và L [180] .
Nếu tính không hòa hợp trong các phân tử sinh học có thể thúc đẩy quá trình đóng gói hiệu quả hơn các đại phân tử trong không gian nội bào hạn chế, thì bất cứ thứ gì có thể tạo ra tính không hòa hợp trong nước (phân tử có nhiều nhất trong tế bào) và / hoặc thúc đẩy quá trình đóng gói phân tử nước hiệu quả hơn bằng cách một số phương tiện khác, cũng có thể làm giảm sự đông đúc nội bào. Các phân tử nước riêng lẻ không phải là bất đối xứng, nhưng kết quả của các nghiên cứu đường hầm-rung-quay-đường hầm bằng tia laser terahertz rộng rãi (VRT) và quang phổ tia laser giữa IR, kết hợp với các tính toán lý thuyết, chỉ ra rằng các máy cắt nước theo chu kỳ và pentamers thực sự không đối xứng [66].
Do đó, ít nhất một số cấu trúc nước siêu phân tử liên kết hydro chuỗi kín do Pang [83,84,86,87] đề xuất cho nước từ hóa (xem thảo luận trong Phần 4C ở trên) có thể là bất đối xứng. Như được đề xuất bởi kết quả của các nghiên cứu hai chiều về các hạt polyme hình tam giác đều, không nằm ngang trong dung dịch nước, sự hình thành các cụm “siêu hạt” không đối xứng cục bộ như vậy dường như được thúc đẩy bởi sự gia tăng entropi tạo ra bởi sự gia tăng chuyển động của các monome bên trong sự sắp xếp bất đối xứng so với điều đó có thể đạt được với sự đóng gói chặt chẽ có trật tự hơn của các hạt riêng lẻ [181]. Dựa trên những cân nhắc này, chúng tôi đề xuất rằng việc hình thành các cụm nước siêu phân tử bất đối, được tạo điều kiện bởi từ trường, có thể giúp giải quyết vấn đề đông đúc trong tế bào.
Một lĩnh vực khác mà chúng tôi nghĩ rằng nước nhiễm từ có thể đóng góp thiết yếu là hỗ trợ quá trình tự lắp ráp sinh học đại phân tử và siêu phân tử. Các thí nghiệm thanh lịch được thực hiện bởi Whitholder và cộng sự đã cung cấp nhiều bằng chứng cho thấy việc sử dụng các lực từ trường, chẳng hạn như trong lực bay từ trường, có thể hướng dẫn sự tự lắp ráp của các cấu trúc ba chiều từ các thành phần nghịch từ thậm chí [182,183].
4.5. Điều chỉnh pha nước: Điều chỉnh hệ thống nước giữa các mặt
Như đã lưu ý trong Phần 2 ở trên, các thí nghiệm với các kỹ thuật quang phổ mới cho phép nghiên cứu các hệ thống sinh học trên quy mô thời gian xuống đến pico giây cho thấy rằng chuyển động quy mô lớn của protein và axit nucleic được xác định bởi sự dao động trong vỏ hydrat hóa, được kiểm soát bởi độ nhớt của dung môi. và hydrat hóa, và không có trong protein đã khử nước [14,17–34,36]. Nếu những thay đổi trong cấu trúc nước giao thoa dẫn đến thay đổi cấu trúc phân tử sinh học, thì các hệ thống sinh học phải có các phương tiện để thay đổi cấu trúc và đặc tính nước giao diện (trong giới hạn hoạt động đúng, cho phép sự sống) để thực hiện một loạt các hoạt động duy trì sự sống của chúng. Trong phần 4C ở trên, chúng tôi đã khảo sát bằng chứng cho thấy từ trường tần số cực thấp có thể làm giảm sức căng bề mặt và tính kỵ nước. Ngoài ra, sự hình thành vi nhũ tương từ tính từ các chất hoạt động bề mặt từ anion đã được báo cáo [184–186]. Những dữ liệu này gợi ý rằng sức căng của nước giữa các bề mặt được điều chỉnh in vivo bởi từ trường và các chất hoạt động bề mặt anion. Thật vậy, kết quả của các nghiên cứu động học phân tử của các ống nano cacbon được flo hóa được đề cập ở trên, chỉ ra rằng hình dạng và khoảng cách giữa các nhóm sulfonat đóng vai trò chủ đạo trong việc xác định tốc độ truyền proton trong các phân tử nước xung quanh [112], gợi ý một cách mà biosulfat trong màng tế bào có thể thực hiện. một chức năng tương tự trong các hệ thống sinh học, và cũng gợi ý một bệnh lý khi mức sulfat bị cạn kiệt.
Màng tế bào thường trở nên tuân thủ hơn (ít “cứng” hơn) khi chúng bị cạn kiệt các biosulfat, chẳng hạn như cholesterol sulfat (Ch-S) và HSPGs, trong các lá ra và glycocalyces của chúng, tương ứng. Màng tế bào tuân thủ tốt hơn (ít “cứng” hơn) tương đối kỵ nước, tức là tương đối “khử mùi” bởi nước giữa các bề mặt. Cuối cùng, các chuyển pha thậm chí, chẳng hạn như sự hình thành hạt nano, có thể xảy ra, đặc biệt là gần điểm ba nơi nước giao thoa sắp đóng băng [142]. Theo lý thuyết Lum-Chandler-Weeks [47], tính kỵ nước tương đối và lý thuyết phân tử về độ mao dẫn [187–189] được dự đoán là sẽ đóng những vai trò chính trong việc xác định sự tuân thủ của tế bào (“độ mềm”) ở cả miền nước nội bào và ngoại bào gần các tấm màng sinh học của chúng tôi. Tốc độ của sóng mao dẫn trên bề mặt có thể được sử dụng để đo sức căng bề mặt, bằng cách chúng tán xạ ánh sáng từ tia laser [189]. Suzuki và cộng sự. đã sử dụng quang phổ điện môi với vi sóng để nghiên cứu quá trình hydrat hóa của tiểu phân đoạn 1 (S1) của myosin. Những thay đổi quan sát được trong quá trình hydrat hóa S1 về mặt định lượng phù hợp với sự thay đổi entropi nhiệt động lớn đi kèm và sự thay đổi nhiệt dung được ước tính bằng phép đo nhiệt lượng, cho thấy rằng sự thay đổi tính kỵ nước của bề mặt protein đóng một vai trò quan trọng trong hiệu ứng bù entanpi-entropy được quan sát thấy trong các bước của quá trình thủy phân S1 ATP [ 190].
Do đó, cần phải mong đợi rằng nhiều, nếu không phải tất cả, sterol có hoạt tính sinh học như các sulfat tương ứng của chúng, có đặc tính amphiphilic cần thiết cho sinh khả dụng. Vitamin D3 sulfat, cholesterol sulfat, DHEA-sulfat, estrone sulfat và các neurosteroid sulfat là những ví dụ [2,191,192]. Ngoài ra, các neurosteroid sulfat dường như hoạt động “từ xa” trong các khớp thần kinh, trái ngược với hoạt động tại các vị trí thụ thể. Do đó, các biosulfat có khả năng hoạt động nhờ ổn định màng tế bào và duy trì CD nước trong không gian ngoại bào. Như đã lưu ý trước đó, các hiệu ứng Grotthuss và Josephson tăng cường có liên quan đến các nhóm CD nước [126,148–150].
Một số chất béo và đồng yếu tố chuỗi trung bình, ví dụ, axit lauric, axit capric, axit ascorbic, axit panthothenic, axit -lipoic và niacin, tất cả đều có chung các đặc tính ổn định màng rõ ràng; Có thể suy luận rằng tất cả chúng đều hoạt động chủ yếu bằng cách hạ thấp sức căng nước giữa các bề mặt. Các polyphenol và polyketon có hoạt tính sinh học đại diện cho các loại chất bắt chước chất hoạt động bề mặt khác, mà hoạt tính sinh học và khả dụng sinh học có thể bị thay đổi đáng kể bởi quá trình sulfat hóa. Resveratrol, curcumin, axit ascorbic và các phenol tăng cường sức khỏe trong cà phê và sô cô la có thể bị sulfat hóa, và đây có thể là chìa khóa cho các lợi ích sinh học của chúng. Các nghiên cứu về chuyển hóa resveratrol cho thấy nó được sulfat hóa trong ruột trước khi hấp thụ [193]. Thực tế là vitamin C xúc tác quá trình chuyển đổi homocysteine thiolactone thành sulfat cũng có thể phụ thuộc vào thực tế là vitamin C cũng có thể bị sulfat hóa [194]. Trong các thí nghiệm in vitro với tế bào chondrocytes, vitamin C được phát hiện là gây ra sự gia tăng 70% trong quá trình sinh tổng hợp các proteoglycan đã sulfat hóa [195], mà chúng tôi đưa ra giả thuyết là do khả năng mang sulfat của nó [196]. Năm 1973, Verlangieri và Mumma đã chứng minh quá trình sulfat hóa cholesterol trong cơ thể bằng acid ascorbic 2-sulfat [197]. Những phát hiện như vậy cho thấy rằng lợi ích sức khỏe của tất cả các phân tử như vậy có thể là do xu hướng tham gia vào quá trình tổng hợp và vận chuyển sunfat của chúng.
Bằng chứng thực nghiệm cho thấy biosunfat được nhúng vào màng có thể có tác dụng có lợi đối với nước bề mặt cho thấy rằng tín hiệu phosphoryl hóa có thể truyền đạt tính năng anion kosmotropic tương tự cho các phân tử liên kết màng. Ngoài ra, người ta cũng biết rằng các tầng tín hiệu phosphoryl hóa được kích hoạt bởi sự suy giảm cholesterol trong màng [198]. Sự suy giảm cholesterol ít nhất có liên quan tuyến tính đến sự giảm cholesterol sulfat trong màng và điều này có thể kích hoạt quá trình phosphoryl hóa các phân tử sinh học màng khác như phosphatidylinositol (PI) thông qua phosphatidylinositol 3 kinase (PI3K), một chất trung gian chính trong các tầng tín hiệu phosphoryl hóa, như một hành động bù đắp. Ba nhóm photphat bổ sung có thể được thêm vào Pi để tạo thành phosphatidylnositol photphat (PIP), phosphatidylinositol bisphosphat (PIP2) và phosphatidyl-inositol trisphosphat (PIP3), được gọi chung là phosphoinositides. PI3K là một chất điều hòa được biết đến trong quá trình hình thành mạch và tăng trưởng khối u [199].
5. Căng thẳng nước giữa các bề mặt ngoại sinh và các hậu quả bệnh lý của nó
Trong các phần trước, chúng tôi đã khảo sát các tài liệu nghiên cứu liên quan đến cấu trúc và đặc tính của nước sinh học có khả năng sống tại các giao diện trong không gian ngoại bào và nội bào. Chúng tôi đã kiểm tra bằng chứng cho thấy sự tương tác của nước giao diện này với các bề mặt kỵ nước và ưa nước và với trường điện từ có thể tạo ra các mạng lưới mở rộng của các dạng nước có cấu trúc, mạch lạc. Các mạng mở rộng này có thể hoạt động như dây hoặc mạch điện cho phép và kiểm soát các quá trình sống (chẳng hạn như chuyển động đại phân tử) bằng cách tăng cường và nhanh chóng hấp thụ, lưu trữ, phát xạ và truyền (dẫn) năng lượng và thông tin. Chúng tôi cũng đã xem xét những cách có thể trong đó cấu trúc và sức căng của nước bề mặt có thể bị thay đổi bởi từ trường và / hoặc chất hoạt động bề mặt anion trên bề mặt màng, cho phép các hệ thống sinh học thực hiện các hoạt động duy trì sự sống thông thường của chúng.
Ngược lại với những biến đổi về cấu trúc và độ căng của nước giữa các bề mặt do các tác nhân nội sinh gây ra như, ví dụ, các ion Ca + 2, Mg2 +, Zn2 +, Co2 +, Mn2 +, cho phép các quá trình sống diễn ra bình thường, chúng tôi sử dụng thuật ngữ “căng thẳng nước ngoại sinh ”(EIWS) để biểu thị một sự gia tăng bệnh lý, có lẽ cấp tính hơn về sức căng nước giữa các bề mặt do tác nhân xenobiotic gây ra. Giá trị sức căng bề mặt gia tăng đã được báo cáo bởi Marcus [200]. Như đã thảo luận đầy đủ hơn trong bài đánh giá trước đây của chúng tôi [2], các tác nhân gây căng thẳng nước giao diện ngoại sinh tiềm ẩn bao gồm các cation kosmotropic như Al3 + và Hg2 +, cũng như các chất hoạt động bề mặt cation và không ion khác nhau. Nếu các hệ thống nước sinh học được coi là các mạch điện mở rộng có thể lưu trữ và truyền năng lượng, thì các tác nhân gây căng thẳng nước ngoại sinh là các tác nhân có thể làm suy yếu và giải phóng năng lượng từ các mạng lưới này bằng cách tạo ra “rò rỉ” hoặc bằng cách tạo ra các mạch ngắn cung cấp thấp hơn đường kháng để xả năng lượng nhanh chóng, do đó làm cạn kiệt năng lượng và gây ra các tổn thương thế chấp dọc theo đường phóng điện. Ví dụ về thiệt hại như vậy sẽ bao gồm sự phá vỡ màng và / hoặc hệ thống protein và / hoặc axit nucleic, tăng tính kỵ nước, tập hợp protein, tập hợp tế bào, tập hợp tế bào vi sinh và sản xuất dư thừa các loại oxy phản ứng, chỉ kể tên một số những kết quả không mong muốn.
5.1. Căng thẳng nước giữa các bề mặt ngoại sinh như một hiện tượng ngắn mạch, giải phóng năng lượng, gây ra tổn thương ngoại bào hoặc nội bào
Trong không gian ngoại bào, bề mặt màng tế bào tích điện âm đặc biệt dễ bị đoản mạch do tương tác với kosmotrope cation hoặc chất hoạt động bề mặt có thể liên kết nhóm sulfat, photphat hoặc cacboxylat lồi ra và phá vỡ hệ thống nước cục bộ. Phù hợp với giả thuyết cạn kiệt năng lượng, khá nhiều tài liệu nghiên cứu gần đây ủng hộ mối quan hệ nghịch đảo giữa ứng suất nước giữa các bề mặt và năng lượng bề mặt [201–206]. Các sóng giữa các mặt đã được xác định bởi các nhà kính hiển vi trong quỹ đạo [207–209]. Gallez và Coakley đã chỉ ra theo kinh nghiệm rằng số lượng sóng trung bình trên một vành tế bào gợn sóng giảm khi điện tích bề mặt tế bào bị cạn kiệt, và khi có mặt thuốc cation, và tăng khi có mặt thuốc dạng anion [198,209]. Do mối quan hệ nghịch đảo giữa bước sóng và năng lượng trong phương trình sóng cổ điển, có thể suy ra rằng sự phân bố trong không gian của mật độ sóng được ghi nhận trên các ảnh hiển vi điện tử quét có thể được tạo ra bởi sự tương tác (phản xạ) của các điện tử với nước có cấu trúc tại giao diện.
Người nhận năng lượng cao nhất cho sự phóng điện đột ngột trong bất kỳ sự cố chập mạch nào gây ra bởi ứng suất nước giữa các bề mặt sẽ là nước giao diện gần đó. Sự phóng điện năng lượng vào mặt nước bề mặt sẽ phá vỡ cân bằng động của nó dẫn đến mật độ giảm và thể tích cao hơn, như khi nước gần bề mặt kỵ nước tiếp xúc với ánh sáng 670 nm [51], như đã đề cập trong Phần 4 ở trên. Nước tỷ trọng thấp hơn có ít khả năng hòa tan các bề mặt kỵ nước. Xu hướng này đã được chứng minh bằng thực nghiệm với nước có chứa protein ubiquitin được “kéo căng” nhân tạo ở áp suất âm trong một sự thích nghi từ Berthelot vào năm 1850 [35,210,211]. Mật độ nước đã giảm từ 1,00 xuống 0,95g/cm3 trong ống cộng hưởng từ hạt nhân (NMR) bằng thủy tinh kín. Protein trong nước “bị kéo căng” này trở nên kém ổn định hơn so với trong nước có tỷ trọng bình thường.
Tương tác kỵ nước tác động đến sự ổn định của nhiều thành phần sinh học và đóng vai trò quyết định trong quá trình gấp protein [212]. Hiệu ứng kỵ nước là một hiện tượng hướng theo entropi phát sinh từ sự khác biệt về mật độ giữa sự sắp xếp theo thứ tự mở của nước trong vùng lân cận của bề mặt không phân cực và nước dạng khối ít có trật tự hơn [58–60,212]. Nếu EIWS làm giảm độ lợi entropi của việc giảm thiểu các bề mặt không phân cực tiếp xúc với nước giao diện, thì cuối cùng nó phải “giết chết” tương tác kỵ nước, do đó làm biến tính protein. Suy luận này được hỗ trợ bởi công trình của Defay và Prigogine, những người đã chỉ ra rằng, ở khoảng giữa pha, điểm ba của nước bị ảnh hưởng bởi độ cong và sức căng bề mặt [213], và bởi lý thuyết Lum-Chandler-Weeks về tính kỵ nước [47 53,55,57,171].
Theo đó, quá trình chuyển đổi in vivo, gel-sol được điều chỉnh bởi sức căng và độ cong bề mặt, như được công nhận ban đầu bởi Prigogine [213,214]. Tuy nhiên, sức căng bề mặt ở giữa các pha có thể bị ảnh hưởng bởi các biến số như sự hiện diện của trường điện từ tĩnh và động, độ bất đối xứng, độ pH và nồng độ của các chất hòa tan, bao gồm cả sự hiện diện của chất hoạt động bề mặt lưỡng tính. Độ nhám và độ cong của màng sinh học rõ ràng có ảnh hưởng lớn đến các đặc tính như độ mao dẫn [189] và lưu lượng máu trong mao mạch [188]. Các đặc tính bất thường của nước siêu lạnh và sự hình thành thủy tinh có thể có mối tương quan in vivo [26,215–219]. Nước ở giai đoạn giữa, trong điều kiện căng thẳng kỵ nước cục bộ cấp tính, được mô tả là “không mong muốn” hoặc “kéo dài” [210], cuối cùng có thể được theo sau bởi sự chuyển pha, có thể tàn phá in vivo [142]. Patel và cộng sự. [53] đã sử dụng các mô phỏng động lực học phân tử để chỉ ra rằng một bề mặt kỵ nước đủ lớn có thể gây ra sự hình thành một mặt phân cách giống như hơi nước, và do đó, xác suất cạn kiệt nước được tăng cường gần bề mặt đó. Các điểm tương đồng được đánh dấu đã được chứng minh giữa giao diện hơi nước và giao diện nước-dầu. Người ta cũng biết rằng các bề mặt kỵ nước hoàn toàn là lực đẩy tạo ra một giao diện giống như hơi-lỏng [47,220,142].
Thiệt hại đối với màng tế bào do căng thẳng nước giữa các mặt có thể làm cho các yếu tố căng thẳng nước giữa dễ dàng tiếp cận với không gian nội bào và gây hại thêm. Tùy thuộc vào tác nhân gây căng thẳng nước giữa các bề mặt và loại bề mặt gặp phải, những tổn thương nội bào như vậy có thể bao gồm sự mở rộng hoặc phân chia sai của protein, phân chia sai DNA và tạo ra các loại oxy phản ứng dư thừa (ROS), làm gián đoạn thêm các hệ thống nội bào. Các loại tổn thương nội bào cụ thể được xem xét dưới đây liên quan đến các hoạt động độc hại của cation nhôm, Al3 +, một chất gây căng thẳng nước ngoại sinh tinh túy có liên quan đến bệnh ung thư vú và bệnh thần kinh, như được thảo luận trong Phần 6 dưới đây. Một con đường bổ sung mà EIWS có thể gây ra tổn thương cả ngoại bào và nội bào được đề xuất bởi kết quả của một nghiên cứu liên quan đến việc xử lý chất tẩy rửa các tế bào nguyên bào sợi của phôi chuột, làm phá vỡ màng tế bào HSPG và liên quan đến chúng như một liên kết giữa chất nền ngoại bào và nội bào. tế bào xương [221]. Dựa trên những phát hiện đã được thảo luận, việc cắt đứt bộ xương tế bào khỏi màng tế bào sẽ định hướng lại bộ xương tế bào về phía nhân tế bào và nhất thiết sẽ có lợi cho đặc điểm phân chia tế bào bệnh lý của bệnh ung thư; một lần nữa, hãy xem Phần 6 để thảo luận thêm.
5.2. Al3 + là cơn ác mộng sinh học
Có rất nhiều tài liệu ghi lại một loạt các tác động độc hại của cation nhôm đối với các hệ thống sinh học. Ở đây chúng tôi xem xét bằng chứng cho năm loại hư hỏng chính do nhôm gây ra: sự dịch chuyển của các cation đơn hoặc hóa trị hai nội sinh thường tạo phức với các phân tử sinh học quan trọng; giảm sinh khả dụng của lưu huỳnh; hành động đông tụ; cảm ứng của quá trình oxy hóa, gây độc gen và căng thẳng cấu trúc protein; và cảm ứng của EIWS.
5.2.1. Sự dịch chuyển của các Cation nội sinh
Al3 + có thể thay thế các cation đơn và hóa trị hai trong các hệ thống sinh học với những hậu quả có hại, như được chỉ ra bởi khả năng ức chế Na + / K + – ATPase, Ca2 + -ATPase, và H + -ATPase [222]. Tuy nhiên, ở đây, chúng ta sẽ tập trung vào một số tình huống cụ thể liên quan đến việc thay thế Ca2 + bằng Al3 +. Ca2 + đóng một vai trò thiết yếu trong sự co cơ [223] và trong một số lượng lớn các con đường tín hiệu tế bào [224]. Do đó, có một tiềm năng lớn đối với Al3 +, hoạt động như một chất bắt chước Ca2 +, trở nên cô lập, trong một quá trình tiêu thụ entropi cấu trúc, ở nhiều vị trí mà nếu không Ca2 + sẽ cô lập, với tác dụng bất lợi.
Al3 + đã được chứng minh là có thể thay thế Ca2 + từ heparan sulfat trong gan chuột [225]. Bằng cách tương tự, có vẻ như Al3 + cũng có thể thay thế Ca2 + từ HSPG khắp cơ thể con người, bao gồm cả những chất được tìm thấy trong dạ dày, ruột non, tuyến tụy, cơ [226], cũng như trong lysosome [227], bộ máy Golgi, và glycocalyces của màng plasmalemmal, bao gồm màng ty thể và màng tế bào thần kinh của não người.
Môi trường tiếp xúc với kim loại được biết đến như là chất nhạy cảm đối với các hiện tượng xuất huyết huyết khối và làm tan huyết khối [228,229]. Do đó, chúng tôi đưa ra giả thuyết rằng Al3 +, có thể kết hợp với nhiều cation kim loại ngoại sinh khác, gây nhạy cảm cho quá trình vôi hóa di căn và quá trình calciphylaxis. Calciphylaxis là một tình trạng chưa được chẩn đoán là quá mẫn cảm toàn thân, trong đó các mô phản ứng với các tác nhân thách thức thích hợp với sự vôi hóa cục bộ đột ngột, nhưng đôi khi phát sinh [228,230]. Vôi hóa di căn là tình trạng tích tụ nhiều cặn canxi photphat khác nhau trong các mô bình thường [231]. Nó thường bắt đầu khi sản phẩm của nồng độ canxi và phosphate trong huyết thanh tính bằng mg / dl vượt quá 70, nhưng đã được báo cáo là đôi khi xảy ra khi sản phẩm này ở dưới ngưỡng này [232]. Dựa trên những quan sát này và kết quả của các nghiên cứu về hydrat hóa ion trước đó của Guo và Tielrooij, chúng tôi gợi ý rằng trong quá trình biến đổi, trước khi vôi hóa di căn, các cặp ion nhôm / photphat và nhôm / sunfat khác nhau vượt quá ngưỡng sức căng bề mặt gia tăng gây rối loạn tín hiệu sinh học , in vivo [233,234], rất có thể bằng cách tạo ra sự mất nước tương đối và không sinh ra của loại được đề cập trước đó [142]. Chuỗi sự kiện được đề xuất này sẽ là một phần của hiện tượng chung mà chúng tôi mô tả là EIWS. Dữ liệu thực nghiệm gần đây của Marcus, chỉ ra rằng Al3 + có tác động tiêu cực đối với sức căng nước giữa bề mặt [200,235], cung cấp hỗ trợ đáng kể cho giả thuyết EIWS [2].
5.2.2. Giảm khả dụng sinh học của lưu huỳnh
Cation Al liên kết mạnh với cystein trong albumin huyết thanh trong máu. Sự hấp thụ cation Al vào albumin huyết thanh có ảnh hưởng sâu sắc đến điện thế zeta [236], thậm chí đưa nó đến giá trị dương ở pH sinh lý với nồng độ nhôm hydroxit vừa đủ. Cũng cần lưu ý, Li (1992) đã chỉ ra rằng điện tích của bong bóng thể hiện “các đặc điểm điện tích bề mặt dương bất thường” trong các dung dịch của các cation Al hóa trị ba [237]. Phân tích kết quả của họ chỉ ra rằng sự đảo ngược của điện tích bong bóng có thể là do sự hấp phụ cụ thể của Al3 + và các phức hydroxo của nó tại mặt phân cách khí-lỏng trong khoảng pH thấp và sự kết tủa của nhôm hydroxit trong khoảng pH trung gian. Sulfate chịu trách nhiệm liên kết với các cation metalloneurotoxin [238] như thủy ngân và Al và đào thải chúng qua thận [239]. Tuy nhiên, hành động như vậy cũng dẫn đến giảm sinh khả dụng của sulfat hơn nữa.
5.2.3. Hành động đông tụ: Các quan sát liên quan từ Hóa học lọc nước
Từ công nghệ lọc nước và xử lý nước thải, người ta đã biết rõ rằng điện thế zeta (ZP) giảm (trở nên ít âm hơn) theo nồng độ của phèn trong khi sự đông tụ của các hạt keo có mối quan hệ hai pha với nồng độ của phèn [240,241]. Áp chế hai lớp có thể đạt được bằng cách tăng cường độ ion của dung dịch bằng cách bổ sung các loại ion bổ sung, tốt nhất là các ion có hóa trị cao. Vì lý do này, các hóa chất điển hình được sử dụng trong quá trình áp chế hai lớp là những hóa chất tạo ra cation có điện tích lớn như Al3 + và Fe3 +. Vì vậy, các hóa chất như Al2 (SO4) · 14H2O (phèn) và FeCl3 thường được sử dụng làm chất đông tụ. Các muối này cũng tạo ra sự đông tụ vì khả năng khử điện tích và tạo cầu nối. AlCl3 và Al2 (SO4) 3 là những chất đông tụ thường được sử dụng chống lại các chất keo âm với sức mạnh đông tụ tương đối là 1000 và> 1000, so với sức mạnh đông tụ của NaCl và Na2SO4 [241].
Các muối Al hiệu quả nhất trong vai trò chất đông tụ là Al2 (SO4) 3 · 14H2O hoặc Al2 (SO4) 3 · 18H2O (phèn chua). Theo Droste [242], khi được thêm một lượng đáng kể, các ion từ các muối này phản ứng với OH¯ hoặc các ion bicacbonat và cacbonat trong dung dịch để tạo ra các hydroxit không hòa tan tương ứng (Al (OH) 3 hoặc Fe (OH) 3). Khi xảy ra kết tủa các hiđroxit thì quan sát thấy hiện tượng đông tụ của các chất keo. Độ hòa tan của Al (OH) 3 là một chức năng của pH, và do đó pH của đông tụ là rất quan trọng [241,242]. Sự kết tủa của các hydroxit Al diễn ra thông qua việc hình thành các hydrocomplex cao phân tử, các hydro này mang điện tích dương nếu độ pH thấp hơn điểm đẳng điện của chúng. Do đó chúng bị hấp phụ trên bề mặt của chất keo tạo ra sự đông tụ và triệt tiêu điện tích. Độ kiềm không đủ cho phép độ pH giảm xuống mức mà ion nhôm trở nên hòa tan cao [241].
Các tấm màng sinh học của chúng ta chủ yếu mang điện tích âm, với mật độ điện tích âm thuần, nhờ các nguyên tố hyaluronat, photphat và biosulfat ở giữa pha nước. Hơn nữa, độ pH được cho là có tính axit gần với pha nước [7] nơi lăng kính nguyên sinh của các tổ hợp phân tử nano của nước CD tạo ra sự phân tách điện tích, động, phạm vi dài bằng hiện tượng Grotthuss [103–106,108], Độc tính vivo của nhôm sunfat ngậm nước đối với cơ thể chúng ta, cho dù uống, tiêm hay bôi tại chỗ, có thể được chứng minh là tự xúc tác và toàn thân, do có sự can thiệp với hiện tượng Grotthuss và hiện tượng Josephson [243,244]. Nói cách khác, nhôm hydroxit không hòa tan có thể dễ dàng tạo thành kết tủa floc chịu trách nhiệm loại bỏ chất keo in vivo, thông qua phản ứng sau [241,242]:
Al2 (SO4) 3 18 H2O + 6H2O 2Al (OH) 3 + 6H + + 3SO42− + 18 H2O (1)
Các ion kim loại đa hóa trị như ion Al tạo thành kết tủa rất ít hòa tan với sự có mặt của các ion photphat. Phản ứng có liên quan đến sự kết tủa photphat là [241]:
Al2 (SO4) 3 · 14H2O (phèn chua) + 2PO4−3 2AlPO4 + 3SO4−2 + 14H2O (2)
Dựa trên dữ liệu xử lý nước thải nói trên [241,242], chúng tôi khá ấn tượng rằng, trong số tất cả các sunfat kim loại được phân tích bởi Pogue và cộng sự, cho đến nay, nhôm sunfat cho thấy khả năng lớn nhất để tạo ra các loại oxy phản ứng nội bào (ROS) [ 245], và do đó, có khả năng đóng góp lớn nhất về mặt di truyền biểu sinh đối với rối loạn chức năng thần kinh sinh ROS và rối loạn chức năng thần kinh qua trung gian ROS [245].
5.2.4. Cảm ứng quá trình oxy hóa, gây độc gen và căng thẳng phù hợp với protein
Al gây ra sự bùng nổ oxy hóa, hoạt động của NADH peroxidase ở thành tế bào và làm tổn thương DNA ở thực vật [246–248]. Một số vắc-xin được bán trên thị trường hiện nay có chứa muối Al làm tá dược với số lượng gần miligam [249], và chúng đã được sử dụng rộng rãi làm tá dược trong bảy thập kỷ qua. Bài đánh giá của Exley (2012) thảo luận về các phức DNA Al và trình bày dữ liệu hỗ trợ cho cation Al gây ra stress oxy hóa như một chất ủng hộ oxy hóa mạnh [250,251], in vivo [252], bao gồm cả sự hình thành có thể có của các phức cation gốc bán khử Al superoxide, trong vivo. Công trình nghiên cứu của Exley cũng cho thấy sự hình thành có thể có của phức cation bán khử Al peroxynitrit, in vivo. Tóm lại, ngày nay có một lượng lớn dữ liệu ngày càng tăng cho thấy rằng cation Al tạo ra ứng suất oxy hóa [251,252], ứng suất nhiễm độc gen [245,253], và IWS [2].
Có nhiều tài liệu ủng hộ kết luận rằng Al làm tăng sức căng bề mặt máu, dẫn đến tăng sức căng bề mặt của nước nội bào, ngoại bào và kẽ, dẫn đến IWS [2]. Al ảnh hưởng đáng kể đến sự luân chuyển protein nội bào, rất có thể gây ra các sự kiện thảm khốc cho sự sống của tế bào [254]. Bằng cách liên kết với axit nucleic, Al cản trở quá trình chuyển hóa protein nội bào [236–238]. Điều thú vị là Sin Hang Lee đã xác định được các đoạn DNA của gen HPV-16 L1 không tăng sinh ở dạng không phải B, trong các đại thực bào của máu và lá lách sau khi chết, dường như được bảo vệ khỏi sự suy thoái bằng cách liên kết chắc chắn với tá dược nhôm dạng hạt được sử dụng trong công thức vắc xin [146].
Al đã được chứng minh trong nhiều nghiên cứu để ức chế chức năng hexokinase, bước đầu tiên trong quá trình đường phân. Năm 1979, Womack và Colowick đã chứng minh sự ức chế men và hexokinase não phụ thuộc proton bởi Al trong các chế phẩm ATP [255]. Năm 1984, Lai và Blass đã chứng minh sự ức chế quá trình đường phân của não bằng Al trong não chuột với giá trị IC50 từ 4 đến 9 microM đối với sự ức chế hexokinase của tế bào và ty thể [256]. Năm 1994, Exley và cộng sự. [257] đã chứng minh rằng Al ức chế hoạt động của hexokinase trong ống nghiệm.
Al dường như có tác dụng hiệp đồng tăng cường các nguy cơ gây độc cho thần kinh do florua gây ra [258–261]. Trong các nghiên cứu về Methanosarcina thermophila của Miles và cộng sự, nhôm florua ở dạng AlF3 hoặc AlF4− đã được đề xuất để bắt chước nhóm phosphoryl ở trạng thái chuyển tiếp xúc tác của acetate kinase [262–264]. Xem thêm Hình 9 (bên dưới)
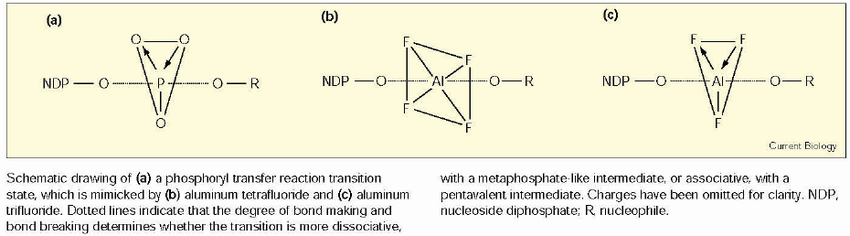
Tái sản xuất từ Wittinghofer (1997) [262] với sự cho phép của Elsevier.
Năm 1993, Maruta và cộng sự đã phân tích phức hợp myosin-ADP-nhôm florua ổn định bằng cách sử dụng 19F NMR. Họ chỉ ra rằng, trong khi liên kết của phức với actin yếu, thì một sự thay đổi cấu trúc riêng biệt đã được tạo ra, cho thấy rằng nhôm florua đóng một vai trò như một chất tương tự photphat [265], càng được chứng thực bởi [266]. Năm 1995, Ponomarev và cộng sự. đã chứng minh rằng nhôm florua tạo phức với ADP hoạt động như chất tương tự trạng thái chuyển tiếp của myosin ATPase, gây ra những thay đổi cấu trúc và ức chế ATPase [267]. Yuan và cộng sự. gần đây đã chỉ ra rằng quá tải Al làm tăng stress oxy hóa (H2O2) ở đồi thị, màng não, tiểu não và thân não ở chuột sơ sinh [268]. Ngoài ra còn có một lượng dữ liệu đáng kể cho thấy rằng không có phạm vi liều thấp hơn có thể dung nạp được mà dưới đó có thể đảm bảo an toàn cho sự tự do khỏi IWS. Haley đã chứng minh rằng sự có mặt của Al làm tăng đáng kể tỷ lệ chết tế bào thần kinh do thimerosal, chất bảo quản chứa thủy ngân vẫn được sử dụng trong nhiều vắc xin đa liều [269]. Với những phát hiện thực nghiệm và lý luận lý thuyết đúng đắn như vậy, chúng tôi đã lập luận rằng nên loại bỏ florua, Al và thủy ngân khỏi nguồn cung cấp thực phẩm vì khả năng tổng hợp biểu sinh, siêu phân tử, độc hại cao, liên quan đến tác động tổng hợp của các ion này lên IWS .
Cation Al3 +, mặc dù là một kim loại không hoạt động oxy hóa khử, là một chất oxy hóa ủng hộ cả trong chế phẩm in vitro và in vivo, tạo điều kiện thuận lợi cho quá trình oxy hóa sinh học do superoxide và sắt [250]. Năm 1992, Fridovich và cộng sự. cho rằng sự tạo điều kiện thuận lợi cho quá trình oxy hóa sinh học theo hướng superoxide bởi Al là do sự tương tác giữa kim loại và anion gốc superoxide [270]. Năm 2009, Pogue et al. dữ liệu được trình bày nhấn mạnh tiềm năng của Al nano trong việc thúc đẩy cơ chế gây độc gen, đặc trưng của các quá trình bệnh thoái hóa thần kinh [253]. Vào năm 2012, Exley đã xem xét hóa học phối trí của Al, bao gồm vai trò của Al như một chất oxy hóa pro, Al như một chất độc excitotoxin và liên kết Al-DNA [252].
5.2.5. Cảm ứng căng thẳng nước giữa các mặt
Mặc dù các cơ chế gây độc của Al vẫn chưa được làm sáng tỏ hoàn toàn, một số nghiên cứu thuyết phục đã được công bố [252,271–273]. Burrell và Exley [272] đã báo cáo mối liên hệ rõ ràng giữa độc tính ở trẻ sơ sinh và tiếp xúc với Al qua đường tiêm. Quá tải Al có liên quan đến thiếu máu. Sự ức chế tế bào tiền thân hồng cầu của Al đã được chứng minh bằng cả xét nghiệm trong vivo. Những thay đổi nghiêm trọng về hình thái của hồng cầu do Al gây ra, và dấu vết của kim loại được phát hiện bên trong các tế bào có hình dạng bất thường [274] hoặc gắn vào màng hồng cầu [275]. Độc tính của Al tiếp tục là một vấn đề đối với bệnh nhân chạy thận nhân tạo mãn tính. Vittori và cộng sự báo cáo sự xuất hiện của hồng cầu có hình dạng bất thường, trong đó một lượng lớn Al được tìm thấy gắn vào màng tế bào [271]. Hồng cầu người ủ lâu dài với Al gây ra các dấu hiệu ngoại hóa hồng cầu ― phosphatidylserine, tăng canxi nội bào và thoái hóa dải 3.
Như đã đề cập trước đó, Al gây ra sự bùng nổ oxy hóa, hoạt động của NADH peroxidase, và tổn thương DNA ở thực vật [246–248]. Dữ liệu đã được trình bày cho thấy rằng Al nguyên nhân tạo hồng cầu NOS, can thiệp vào quá trình tổng hợp sulfat, có thể bằng cách dịch chuyển kẽm trong khoang hình thành giữa hai monome của phân tử [2,276]. Sự gián đoạn này dẫn đến việc sản xuất peroxynitrit thông qua phản ứng của superoxit với oxit nitric. Vào năm 2011, Kawahara và Kato-Negishi đã cung cấp một bảng tham khảo kỹ lưỡng tóm tắt các tác động của Al đối với hệ thần kinh trung ương, bao gồm các tác động bất lợi lên hạt nhân và biểu hiện gen, chức năng tế bào, lipid màng và các chức năng cao hơn [222]. Nếu cation gốc bán khử Al-superoxide (và / hoặc phức hợp Al-peroxynitrite) được gợi ý bởi Exley (2012) được hình thành, thì một cơ chế gây ra stress oxy hóa và nhiễm độc gen có thể là di chứng bất lợi [252].
6. Ứng dụng EIWS cho các bệnh lý cụ thể
Với tất cả những điều đã nói ở trên, các giả thuyết và bằng chứng từ Phần 4 và 5, liên quan đến nước có cấu trúc hỗ trợ sự sống tại các giao diện sinh học và căng thẳng nước ngoại lai, có thể được áp dụng cho căn nguyên của một số trạng thái bệnh cụ thể, bao gồm ung thư vú, bệnh thần kinh. , và bệnh truyền nhiễm. Mục đích là để chứng minh, với những ví dụ cụ thể này, giả thuyết trung tâm của chúng tôi về EIWS là nguyên nhân chính dẫn đến sự phát triển của bệnh được chứng minh bằng nhiều bằng chứng từ các tài liệu.
6.1. Ung thư vú
Dựa trên những điều đã nói ở trên, có vẻ như đặc điểm phân chia tế bào bệnh lý của bệnh ung thư được kết tủa bởi sự thay đổi cấu trúc và độ căng của nước giữa các bề mặt. Vào năm 2011, Abramczyk và cộng sự đã trình bày những hình ảnh “sinh thiết quang học” đầu tiên của Raman về mô vú người không ung thư và ung thư (ung thư ống dẫn lưu thâm nhiễm) [277]. Sự chuyển dịch màu đỏ rõ rệt của vị trí đỉnh tối đa của chế độ kéo dài OH đã được quan sát xác nhận rằng các đặc tính dao động của nước giao diện quan sát được trong các môi trường sinh học hạn chế khác hẳn so với các đặc tính trong môi trường nước lớn.
Như đã đề cập trong Phần 2 ở trên, kết quả nghiên cứu MRI chỉ ra sự khác biệt đáng kể về cấu trúc nước trong tế bào bình thường và tế bào ung thư, trong đó nước dường như có cấu trúc ít hơn trong tế bào khối u [7-9]. Phù hợp với các phát hiện MRI, các nghiên cứu bằng kính hiển vi lực nguyên tử (AFM) chỉ ra rằng các tế bào ung thư vú, buồng trứng, phổi và tuyến tụy “mềm” hơn (“tuân thủ” hơn) so với các tế bào bình thường tương ứng [278–280]. Kết quả của các nghiên cứu microfluidics gần đây cho thấy mối tương quan chặt chẽ giữa độ ác tính (khả năng di căn) và tính linh hoạt của tế bào ung thư vú; “tế bào khởi phát khối u” được mô tả là cho thấy “khả năng biến dạng giống tế bào gốc” [281].
Swaminathan và cộng sự. đã chứng minh rằng tế bào ung thư có tiềm năng xâm lấn lớn nhất ít cứng hơn tế bào có tiềm năng thấp nhất năm lần, và các phương pháp dược lý để giảm độ cứng của tế bào làm tăng khả năng xâm lấn [282]. Sự giảm độ cứng của màng tế bào ung thư đã được chứng minh thông qua công nghệ AFM liên quan đến sự phá vỡ các vi ống do tiếp xúc với nocodazole [218], dẫn đến sự gián đoạn trong vận chuyển lipid và chức năng caveolin [100]. Có thể suy ra rằng nhôm cũng phá vỡ các vi ống, dẫn đến đặc tính “mềm” quan sát được. Thật vậy, người ta đã chứng minh rằng nhôm phá vỡ các vi ống trong thực vật [283]. Kiểm tra tổ chức tế bào trong nuôi cấy tế bào ung thư vú trong ống nghiệm cho thấy một loại tế bào ung thư có đặc điểm là hình tròn nhỏ, mọc thành từng đám nhiều lớp. Các tế bào có hình thái và đặc điểm tăng trưởng này bị nghèo đi nghiêm trọng trong các vi ống [284]. Các nghiên cứu của Beall và cộng sự [9,284] đã chỉ ra rằng trạng thái ung thư có liên quan đến sự gia tăng tự do chuyển động của các phân tử nước, và rằng các tế bào phát triển chậm nhất đã chứng minh khả năng di chuyển của nước bị hạn chế hơn, cùng với mạng lưới vi ống polyme hóa phong phú hơn. Do đó, sự phá vỡ cấu trúc tế bào dường như là một tính năng đặc trưng của kiểu hình ung thư vú.
Trong khi các tế bào ung thư ác tính nhất “mềm” hơn các tế bào bình thường, thì mô ung thư (ECM) bao quanh các tế bào này thường cứng hơn mô bình thường [285]. Dữ liệu từ cả nghiên cứu thực nghiệm và nghiên cứu tính toán chỉ ra rằng sự mất nước của collagen, protein ECM chính, làm tăng độ cứng của nó [286]. Karamichos (2007) đã chứng minh bằng thực nghiệm rằng việc tăng độ cứng của ma trận collagen đã làm chậm đáng kể sự khởi phát và giảm lượng lực cơ học (sức căng) tạo ra bởi tế bào chủ [287], trong ống nghiệm. Kết quả của cả nghiên cứu lý thuyết và thực nghiệm ủng hộ đề xuất rằng lực căng của tế bào có liên quan nghịch với khả năng biến dạng của nó như được mô tả ở trên [288,289]. Do đó, việc giảm sinh lực theo báo cáo của Karamichos và các đồng nghiệp ngụ ý rằng độ cứng của ma trận collagen cao hơn đã đẩy các tế bào đến trạng thái giống ung thư hơn. Quan sát của họ rằng các tế bào trở nên tách rời và phát triển hình thái tròn khi bị bỏ đói (thông qua việc loại bỏ môi trường phát triển huyết thanh của thai nhi) phù hợp với giả thuyết này, vì sự gia tăng độ tròn (mất tính dị hướng) cũng đã được báo cáo đối với các tế bào ung thư trong các nghiên cứu MRI ( sẽ được thảo luận trong Phần 6.2 dưới đây).
Trong vòng một thập kỷ qua, một loạt các thí nghiệm đã được tiến hành để xem liệu mục tiêu của chất gây ung thư nằm trong biểu mô hay trong mô đệm (mô liên kết) của tuyến vú [290–292]. Thực nghiệm đã quan sát thấy rằng sự tái tổ hợp mô của stroma tiếp xúc với chất gây ung thư với các tế bào biểu mô bình thường không bộc lộ dẫn đến tân sinh, trong khi sự kết hợp ngược lại thì không, cho thấy rằng stroma, chứ không phải các tế bào riêng lẻ trong biểu mô, là mục tiêu của chất gây ung thư [ 290]. Sau đó, khi các tế bào khối u được cấy vào chuột ở các độ tuổi khác nhau, quan sát thấy rằng ở chuột trưởng thành, các tế bào khối u đó tạo ra các ống tuyến vú bình thường về mặt kiểu hình, do đó thiết lập khả năng “bình thường hóa” (tức là đảo ngược) kiểu hình khối u của tế bào tuyến vú chuột. [291]. Như Sonnensheim và Soto đã chỉ ra, những kết quả này phù hợp với lý thuyết trường tổ chức mô (TOFT) và thách thức lý thuyết đột biến soma (SMT) [293, tr. 91]. Theo TOFT, lần đầu tiên được đề xuất bởi Sonnenschein và Soto vào năm 1999 [294], sự tăng sinh và vận động, với tư cách là các đặc tính cấu thành, chiếm ưu thế của tất cả các tế bào, được cho là đại diện cho trạng thái mặc định của tất cả các tế bào. Kiến trúc mô bị thay đổi tạo điều kiện thuận lợi cho sự biểu hiện của hai trạng thái cấu tạo này liên quan trực tiếp đến sự phát triển và di căn của khối u. Hơn nữa, TOFT cho rằng sinh ung thư, như sinh mô (hình thành mô) và sinh cơ (hình thành các cơ quan), là một hiện tượng siêu tế bào, có nghĩa là nó xảy ra ở cấp độ mô của tổ chức sinh học. Do đó, theo TOFT, hợp lý để kết luận rằng sự khác biệt quan trọng giữa tế bào gốc và tế bào ung thư là sự phát triển đã trở nên tồi tệ [295].
Một số nghiên cứu đã liên kết ung thư vú với cation nhôm – một tác nhân gây căng thẳng nước ngoại sinh “cổ điển” như đã thảo luận trong Phần 5 ở trên ― mặc dù chưa có nghiên cứu nào đề xuất được cơ chế thuyết phục mà nhôm có thể gây ra hoặc góp phần gây ra bệnh ung thư đó. Silva và cộng sự. (2012) phát hiện ra rằng các kim loại sau đây có khả năng liên kết với các thụ thể estrogen của tế bào và sau đó bắt chước hoạt động của các estrogen sinh lý: “nhôm, antimon, arsenit, bari, cadmium, crom (Cr (II)), coban, đồng, chì, thủy ngân, niken, selente, thiếc và vanadate ”[296,297]. Al gần đây đã được xác định trong mô ung thư vú [298,299], với nồng độ cao hơn đáng kể ở phần tư phía trên bên ngoài của vú so với các vùng bên trong (giữa và giữa). Năm 2012, Sappino et al. [299] phát hiện ra rằng, trong MCF-10A tế bào biểu mô tuyến vú ở người, một mô hình tế bào biểu mô tuyến vú bình thường ở người, tiếp xúc lâu dài với nồng độ nhôm clorua (AlCl3) 10–300 μM, tức là thấp hơn tới 100.000 lần so với những chất được tìm thấy trong chất chống mồ hôi, và trong phạm vi của những chất được đo gần đây ở vú người, dẫn đến mất khả năng ức chế tiếp xúc và tăng trưởng không phụ thuộc vào mỏ neo. Phát hiện này sẽ đóng vai trò là một cảnh báo trọng điểm rằng việc phơi nhiễm Al trong môi trường [252] từ chế độ ăn uống [300], đường tiêm [301] và tại chỗ [302], có thể gây ra hậu quả gây ung thư [299,303] và biểu sinh [245,253].
Ngoài việc khảo sát các tác động bệnh lý của cation nhôm như một tác nhân gây căng thẳng nước giao diện ngoại sinh tinh túy trong Phần 5 ở trên, chúng tôi cũng đề cập đến một lộ trình bổ sung mà EIWS có thể làm phát sinh sự phân chia không kiểm soát. Các thí nghiệm được báo cáo vào năm 1985, liên quan đến việc xử lý tẩy rửa các tế bào nguyên bào sợi của phôi chuột, dẫn đến sự phá vỡ HSPG của màng tế bào, do đó liên quan đến các biosulfat này như một liên kết thiết yếu giữa chất nền ngoại bào (ECM) và bộ xương nội bào [221]. Như đã nói ở trên, kết quả là sự ngắt kết nối của bộ xương tế bào khỏi màng tế bào có thể chuyển hướng bộ xương tế bào về phía nhân tế bào và dẫn đến sự phân chia tế bào ung thư. Hỗ trợ cho giả thuyết này được cung cấp bởi các nghiên cứu của Kanthou và Tozer [304], những người đã báo cáo rằng các tế bào nội mô của con người tiếp xúc với một yếu tố gây căng thẳng nước ngoại sinh, combretastatin A-4-phosphate, hình thành các blu (phình cục bộ trong màng sinh chất do tách của bộ xương tế bào), tiếp theo là sự gián đoạn trong các vi ống và bộ xương tế bào cuối cùng có những tác động bất lợi cao đến khả năng tồn tại của tế bào. Ngoài ra, các nghiên cứu quang phổ điện môi vi sóng, spin-echo 1H-NMR trường xung, và quang phổ huỳnh quang đã phát hiện ra sự gia tăng tính linh động của nước — ngụ ý cấu trúc nước giảm — xung quanh thành phần F-actin của xương tế bào [305,306].
Theo Pollack, khi quá trình nguyên phân và tế bào diễn ra nhanh chóng ngoài tầm kiểm soát, kết quả không may là ung thư. Liên quan đến việc phát triển giả thuyết trung tâm của chúng tôi, ông tiếp tục nói ở trang 221, “một môi trường nước bị rối loạn do đó có thể tạo điều kiện cho nguyên phân – tế bào sẽ thiên về sao chép” [7]. Ông dự đoán một liệu trình điều trị có thể chứng minh hiệu quả, liên quan đến nước, khi ông tuyên bố rằng các tác nhân thúc đẩy trật tự nước được dự đoán sẽ ức chế sự tăng sinh của khối u. Các phát hiện được báo cáo trong bài báo này hỗ trợ kết luận của Pollack. Phương pháp điều trị mà ông khuyến nghị phù hợp với hy vọng làm giảm EIWS bằng cách khôi phục và bảo tồn tiêu thụ entropy cấu trúc [139–143].
6.2. Bệnh thần kinh
Hình ảnh căng dây khuếch tán (DTI) là một kỹ thuật MRI được phát triển gần đây có thể đo lường các đặc tính vật lý cấp độ phân tử và vĩ mô của nước giao thoa, in vivo, không xâm lấn. Ước tính DTI cung cấp thông tin vô hướng (dị hướng phân đoạn, độ khuếch tán trung bình) và bản đồ vectơ có thể cung cấp các cơ chế tương phản bổ sung cho các cơ chế tương phản của MRI thông thường [307]. Mối quan tâm đặc biệt là một đại lượng vô hướng được gọi là dị hướng phân số (FA), dùng để chỉ mức độ hạn chế theo hướng của sự khuếch tán: giá trị FA bằng 1 tương ứng với sự khuếch tán bị giới hạn ở một hướng, trong khi giá trị FA bằng 0 biểu thị quá trình khuếch tán được hạn chế như nhau hoặc không bị hạn chế ở tất cả các hướng. Các đánh giá về cơ sở vật lý và tài liệu đang phát triển về các ứng dụng tiền lâm sàng và lâm sàng của DTI ở các cơ quan khác nhau, bao gồm não và tủy sống, đã được viết [307–312], và dựa trên kết quả được báo cáo ở đây là hợp lý để suy luận rằng Tính dị hướng phân đoạn (FA) được ghi nhận trên ảnh DTI ở các trạng thái sức khỏe khác nhau có thể được giải thích bởi sự khác biệt về hành vi của các phân tử nước gần bề mặt ưa nước và kỵ nước, như Despa đã lưu ý [60]. Đặc biệt hơn, sự khác biệt về FA được thấy trong các nghiên cứu DTI về bệnh lý thần kinh và ung thư so với đối chứng khỏe mạnh, có thể được quy trực tiếp cho sự khác biệt trong hành vi của các phân tử nước tại các vị trí ưa nước so với các vị trí kỵ nước, kết quả ròng có thể là do sự phá hủy cấu trúc của nước giao diện ở giữa các pha của mô đang được nghiên cứu.
Tiềm năng của DTI đối với nghiên cứu khoa học thần kinh cơ bản là đáng kể và vẫn đang tiếp tục phát triển, nhưng các nghiên cứu DTI về mô não ở những bệnh nhân mắc nhiều chứng rối loạn thần kinh đã mang lại kết quả đáng kể. Năm 2004, Barnea-Goraly và cộng sự quan sát thấy giá trị FA giảm trong một nghiên cứu sơ bộ về cấu trúc chất trắng ở những người mắc chứng tự kỷ [313]. Một nghiên cứu DTI tiếp theo liên quan đến trẻ tự kỷ ở độ tuổi đi học cho thấy giảm đáng kể FA và suy giảm cấu trúc vi chất trắng, có thể liên quan đến giảm kết nối trong tiểu thể, nang trong, tiểu não trên và tiểu não giữa [314]. Vào năm 2006, DTI đã được sử dụng để chỉ ra rằng sự giảm dị hướng nổi bật nhất ở vùng trán và thân, và đặc biệt lan rộng ở vùng chất trắng phía trước ở bệnh nhân tâm thần phân liệt [315,316]. Năm 2010, Friese et al. cung cấp các phân tích đa biến để chỉ ra rằng dữ liệu hình thái dựa trên biến dạng (DBM) và DTI có thể được sử dụng để phân biệt giữa những người tham gia khỏe mạnh và bệnh nhân mắc bệnh Alzheimer với độ chính xác tương đương [315,317,318].
Năm 2010, Inglese và Bester sử dụng MRI có trọng số khuếch tán để nghiên cứu bệnh nhân đa xơ cứng (MS) [319]. Năm 2007, Agosta et al. đã sử dụng DTI để thu được thông tin về độ khuếch tán trung bình (MD) và FA trong việc đánh giá tổn thương dây cổ tử cung ở bệnh nhân MS [320]. Năm 2002, Cercignani và cộng sự. sử dụng phép đo DTI của MD, FA và sự gắn kết giữa các voxel trong các tổn thương MS và chất trắng xuất hiện bình thường (NAWM) [321]. Điều thú vị là vào năm 2004, Law et al. đã chứng minh rằng NAWM của những bệnh nhân bị MS tái phát tái phát (RRMS), cho thấy giảm tưới máu so với nhóm chứng [322] bằng cách sử dụng hình ảnh cộng hưởng từ tưới máu tăng cường độ nhạy cảm động (MR). Năm 2012, Hasan et al. đã sử dụng DTI định lượng trong nghiên cứu về sự thoái hóa thần kinh mô não ở bệnh nhân MS [323] với tổn thương do tổn thương và thoái hóa thần kinh trong bệnh MS tái phát (RRMS). Bệnh lý não lan rộng và thành phần tổn thương thoái hóa thần kinh độc lập với các tổn thương trong RRMS đã được chứng minh.
Vì tính dị hướng khuếch tán cung cấp thông tin giải phẫu và phân tử vi mô (cấp độ tế bào) liên quan đến các đặc tính của nước giữa các mô trong mô, các nghiên cứu DTI nêu trên về chứng tự kỷ, tâm thần phân liệt, bệnh Alzheimer và bệnh đa xơ cứng đều cho thấy rằng nước giao thoa đang trở nên tương đối bị hủy hoại sớm trong quá trình thoái hóa thần kinh. hoặc quá trình bệnh thần kinh miễn dịch. Cần nhấn mạnh rằng các đặc tính lý sinh của nước trong mô chịu trách nhiệm trực tiếp cho các thông số DTI đo được. Trạng thái lý sinh của nước giao diện trong các mô là những gì thực sự đang được đo. Quan trọng là, quan sát rằng dị hướng trước quá trình tạo myelin [307] ủng hộ quan điểm rằng cấu trúc nước giữa các bề mặt là yếu tố chủ yếu ảnh hưởng đến tính thấm của màng tế bào, sự tạo myelin, tính toàn vẹn của sợi trục và sự phân chia. Dựa trên luận điểm trọng tâm đó, cần phải dự đoán rằng, trong nhiều bệnh thoái hóa thần kinh và miễn dịch thần kinh, mất tính dị hướng, mất độ cong, tăng cường độ khuếch tán và mất độ cứng (mềm), được cho là trực tiếp do sự phá hủy của nước giao thoa. trước các dấu hiệu và triệu chứng rõ ràng của bệnh ung thư, thần kinh và bệnh truyền nhiễm.
6.3. Bệnh truyền nhiễm
Ngày càng có nhiều bằng chứng trong các tài liệu cho thấy căng thẳng nước ngoại sinh giữa các môi trường (EIWS) thúc đẩy các bệnh truyền nhiễm. Rõ ràng là các tác nhân truyền nhiễm chỉ lợi dụng những thiệt hại đối với môi trường sinh học do EIWS gây ra. Thiệt hại do EIWS gây ra này có thể bao gồm sự tập hợp và / hoặc tập hợp sai của protein như biểu hiện trong các bệnh prion [324,325], cũng như tạo điều kiện cho quá trình dung hợp màng mà vi khuẩn gây bệnh, vi rút hoặc thậm chí prion (protein bị gấp khúc bệnh lý) xâm nhập vào vật chủ tế bào. Cả hai loại thay đổi bệnh lý làm giảm khả năng chống nhiễm trùng này được xem xét chi tiết hơn dưới đây.
Cấu trúc ba chiều được sử dụng bởi các peptit và protein không chỉ phụ thuộc vào trình tự chính mà còn phụ thuộc vào các điều kiện như độ phân cực của dung môi. Dung môi hydrat hóa động, tức là, các cụm nano tổng hợp của nước từ hóa, phần lớn quyết định cấu trúc peptit và protein. Năm 1996, Kuntz và cộng sự. giả thuyết rằng trạng thái cấu trúc của peptit là một chuỗi xoắn alpha đơn phân và một tấm beta phản song song tổng hợp. Các điều kiện khuyến khích tổng hợp có xu hướng ưu tiên trang tính; các điều kiện không khuyến khích sự kết hợp có xu hướng ưu tiên chuỗi xoắn. Họ gợi ý rằng việc xem xét các thay đổi cấu trúc phụ thuộc vào dung dịch có thể ảnh hưởng đến các quá trình sinh học nhất định [326]. Lý thuyết của họ phù hợp với những phát hiện và lý thuyết được báo cáo ở đây. Như đã thảo luận trong Phần 4 và 5 ở trên, bằng chứng chỉ ra hiệu ứng kỵ nước do nước điều khiển đóng vai trò chính trong việc xác định cấu trúc protein và liên kết protein-protein [58–60,212]. Một giả thuyết khác liên quan đến “quá trình hydrat hóa phân cực bị cản trở một phần” của xương sống protein đã được đề xuất bởi Fernandez [205,206,327,328]. Mặc dù Fernandez đã hợp lý hóa quá trình chuyển đổi từ cấu trúc dạng tế bào (khỏe mạnh) sang dạng phế phẩm (bệnh lý, kiểu prion) bằng cách phân tích mô hình của các liên kết hydro kém khử phân cực (UDHB) [327,328], cả hai cách giải thích hiệu ứng kỵ nước và “cản trở quá trình hydrat hóa phân cực ”Giả thuyết gán một vai trò chi phối cho quá trình hydrat hóa trong việc thúc đẩy cấu trúc protein.
Ngược lại với đề xuất của Fernandez [206], EIWS của loại được cung cấp bởi các chất hoạt động bề mặt cation phải có giá trị ngang bằng nếu không muốn nói là một yếu tố lớn hơn, trong việc tạo ra sức căng bề mặt sinh học có thể thúc đẩy sự kết tụ bất thường của tế bào [2]. Từ lâu, người ta đã biết rằng phèn, một tác nhân gây căng thẳng nước ngoại sinh, làm ngưng kết các tế bào hồng cầu và khiến chúng dễ bị thực bào [329,330]. Các so sánh thực nghiệm đã được thực hiện giữa tác động trực tiếp của các kim loại khác nhau lên tế bào đỏ và khả năng của chúng để hỗ trợ hoặc tăng cường hoạt động của bổ thể [331,332]. Các kim loại đa hóa trị được tìm thấy để tạo thành phức hợp metallo-protein trên màng tế bào hồng cầu đã chứng minh một đặc tính chung là làm thay đổi quá trình hydrat hóa và khả năng phản ứng của màng tế bào và của cấu trúc protein. Al3 +, Th4 +, Fe3 +, Cr3 +, Ce3 +, và Pb2 + (đặc biệt là Fe3 + và Cr3 +) đã được chứng minh là làm cho phế cầu và trực khuẩn thương hàn dễ bị thực bào [329,330]. Mối tương quan đã được quan sát thấy giữa khả năng của các kim loại này và của tannin thực vật đối với vi khuẩn ngưng kết và làm cho chúng dễ bị thực bào [331].
Ngoài việc tập hợp sai protein liên quan cụ thể đến các bệnh prion, sự kết hợp màng tế bào vật chủ với màng tế bào vi khuẩn hoặc vi rút lây nhiễm là một bước thiết yếu trong quá trình lây nhiễm nói chung và phản ứng miễn dịch. Các tổng quan gần đây đã mô tả các tương tác phức tạp của protein /lipid diễn ra trong các sự kiện hợp nhất màng và vai trò của độ cong màng trong việc ảnh hưởng đến khả năng sinh sản [333,334]. Các phép đo lực trực tiếp liên quan đến lớp kép chất hoạt động bề mặt chất béo hỗ trợ suy luận rằng quá trình hợp nhất được thúc đẩy bởi cùng một loại hiệu ứng kỵ nước quyết định cấu trúc protein [335]. Dựa trên thảo luận trong Phần 4 và 5 ở trên, có vẻ như tính nhạy cảm của tế bào chủ đối với sự dung hợp màng được kiểm soát bởi cấu trúc nước giữa các pha gần màng tế bào bên ngoài, với cấu trúc nước này, lại bị ảnh hưởng bởi các tác nhân gây căng thẳng nước ngoại sinh và mức độ quá trình sulfat hóa các HSPG (heparan sulfat proteoglycan) trên bề mặt ngoài của màng.
Các phân tử và ion nhỏ, đáng chú ý nhất là các cation, có thể tạo ra sự dung hợp màng [336], sau đó được trung gian bởi cái gọi là peptit dung hợp như glycoprotein vỏ của vi rút cúm (hemagluttinin, HA0) và vi rút suy giảm miễn dịch ở người (HIV-1; gp160 ) [337]. Cả glycoprotein-41 (gp41) và hemagluttinin-2 (HA2) đều trải qua sự thay đổi cấu trúc thành trạng thái có thể xúc tác sự hợp nhất của vỏ virus với màng tế bào. Có thể suy ra rằng EIWS tạo ra phản ứng protein mở ra (UPR) ở HA và gp41, làm lộ ra các vùng kỵ nước cục bộ, cái gọi là “peptit dung hợp”, bao gồm các vùng lưỡng cực đầu N tiếp xúc, các vùng giàu glycine [337], sau EIWS và UPR, loại trừ nước do hiệu ứng kỵ nước [59,60]. Trình tự thời gian là vật chất vì EIWS, được liên kết nổi bật nhất với các phân tử và cation nhỏ cation, rõ ràng là có trước các bước sớm nhất trong quá trình lây nhiễm và lây nhiễm. Bằng chứng cho thấy rằng EIWS có khuynh hướng lây nhiễm và tạo điều kiện cho khả năng lây nhiễm.
Trong Phần 4 ở trên, chúng ta đã thảo luận về các nghiên cứu được thực hiện với các chất fluoropolyme được sulfo hóa và các tấm ống nano cacbon cho thấy cấu trúc đáng kể của nước gần các loại bề mặt này [72–74,112]. Dựa trên những kết quả đó và báo cáo gần đây về sự gia tăng tính nhạy cảm bị virus herpes tấn công ở các tế bào có mức độ N-sulfat thấp trong lớp HSPG của bề mặt màng ngoài của chúng [338], người ta suy ra rằng các HSPG bị sulfat hóa cao ở bên ngoài bề mặt của màng tế bào đóng một vai trò quan trọng trong việc duy trì cấu trúc nước ngoại bào tạo sự sống và khả năng chống lại sự xâm nhập của nhiễm trùng.
Việc xem EIWS là cơ sở cho tính nhạy cảm với bệnh truyền nhiễm thay đổi các bước cần thực hiện để phòng ngừa và điều trị các bệnh lý đó. Cụ thể, bổ sung mức biosulfate (để giảm căng thẳng nước giữa các bề mặt), hydrosol bạc (để tăng tính tiêu cực của điện thế zeta), ánh sáng mặt trời đầy đủ, uống nước nhiễm từ, nối đất, liệu pháp điện từ và một số chất hoạt động bề mặt lưỡng tính anion (ví dụ: pantothenate, ascorbate, resveratrol, curcumin, axit capric, axit lauric, axit alpha lipoic), có thể giúp ngăn ngừa “nhiễm trùng”. Ngoài ra, cần thận trọng tránh thực phẩm và nước được chiếu xạ bằng lò vi sóng. Do đó, theo luận điểm trọng tâm của bài báo này, khả năng “tiêm chủng điện từ” của loại được giả thuyết bởi Liboff [339], và các chiến lược phòng ngừa và điều trị nhằm mục đích giảm IWS và nâng cao ZP, có ý nghĩa hơn nhiều so với “khóa -key ”sinh học phân tử, liệu pháp gen tâm lý để phòng chống bệnh tật cho con người. Liboff dường như gợi ý rằng liệu pháp điện từ (EMT) cần phải dành riêng cho vi khuẩn. Tuy nhiên, trong khi điều này có thể được chứng minh là đúng, có thể hình dung rằng EMT có thể đơn giản được sử dụng để “nạp năng lượng” cho các KKT và CD nước có cấu trúc của chúng ta. Nếu một phương pháp không xâm lấn, an toàn có thể được phát triển, nhờ đó nước EZ đặc EMT bằng cách tạo ra và bổ sung các cụm nano con quay hồi chuyển đa phân tử của nước từ hóa, thì một phương pháp như vậy có thể cắt đứt con đường phổ biến ban đầu dẫn đến viêm nhiễm, bệnh tật và tử vong [2]. Nếu đúng như vậy, con đường ban đầu của vi rút Ebola [340], hay còn gọi là độc tố rắn cắn, chỉ cần lấy hai ví dụ dễ hiểu, có thể bị chặn sớm, trước khi nó trở thành tổn thương và rối loạn không thể phục hồi.
Tiếp xúc với EIWS cation từ nhôm, thủy ngân, v.v., được cho là chất nhạy cảm đối với hiện tượng huyết khối [228]. Trong bối cảnh nhạy cảm IWS, một vi khuẩn có thể là nguyên nhân gây ra hiện tượng huyết khối tổng quát (THP-G) hoặc trong một số trường hợp, đối với hiện tượng Sanarelli-Shwartzman tổng quát (SSP-G). Theo nghiên cứu và lý thuyết được thảo luận trong bài báo này, vi khuẩn sống trong cơ thể là những kẻ cơ hội, cũng như bất kỳ loại vi rút nào có khả năng lây nhiễm cao. Chặn cổng nhập cảnh bằng cách hạ thấp IWS và nâng cao ZP, dựa trên lý thuyết và nghiên cứu hiện tại có liên quan, có ý nghĩa. Ngược lại, gieo mầm vào bầu không khí bằng các hạt nano nhôm, đưa các chất độc như florua vào nước uống, tiêm muối cho người (chưa kể động vật) với muối nhôm và ethyl thủy ngân, khiến trẻ nhỏ và trẻ nhỏ tiếp xúc với ngày càng nhiều mầm bệnh đã biết, và tiếp tục để nhân lên sự phơi nhiễm độc hại và sự tương tác của chúng thông qua thuốc trừ sâu, chất bảo quản, và các tác động cuối cùng của tất cả những điều đã nói ở trên là không phù hợp với lý thuyết và nghiên cứu tốt nhất hiện nay.
6.4. EIWS và bệnh tật
Dữ liệu NMR, DTI và AFM cho thấy các tế bào ung thư thường mềm hơn, tròn hơn và tuân thủ hơn các mô khỏe mạnh. NMR, DTI, AFM, FTIR, nhiễu xạ tia X, nhiễu xạ nơtron, KITA và quang phổ điện môi cho thấy rằng các đám nano nước có cấu trúc bị phá hủy, ban đầu trong chất nền ngoại bào (ECM) và sau đó là trong tế bào chất, khi các đường dẫn của các vi ống và bộ xương tế bào bị phá vỡ bởi EIWS ― kết tủa bởi các chất hoạt động bề mặt cation hoặc các chất gây căng thẳng đã biết khác [258,228]. Tuy nhiên, luận điểm trọng tâm của bài báo này không mâu thuẫn với khả năng rằng sự gắn kết [341] giữa nước có cấu trúc trong ECM và nước có cấu trúc trong tế bào chất có thể dẫn đến sự phá hủy đồng thời nước ECM và nước trong tế bào chất bởi EIWS [342]. Độ rộng tín hiệu cộng hưởng từ hạt nhân bên trong tế bào bình thường rộng hơn nhiều, cho thấy nước nội bào có cấu trúc hơn nhiều so với nước ngoài tế bào hoặc nước tinh khiết [343]. Tuy nhiên, mối quan hệ của nước trong tế bào và bộ xương tế bào đã được xem xét lại [344]. Lượng nước “tự do” so với nước “liên kết” [345], ion K + và bộ xương tế bào đều liên quan đến sự khác biệt giữa tế bào bình thường và tế bào ung thư [346]. Do đó, có thể suy ra rằng sự khác biệt quan trọng giữa tế bào bình thường và tế bào ung thư nằm ở sự mất cân bằng tinh vi về sức căng nước giữa nội bào và ngoại bào. Kết hợp với giả thuyết Cảm ứng liên kết của Gilbert Ling [347] và giả thuyết tổng hợp gốc của Matveev [348], ở đây có thể suy ra rằng cấu trúc nước bị thay đổi bởi các phân tử sinh học cũng như bởi các thực thể gây bệnh như một số ion solvat hóa, và đến lượt nó là nước động lực học và cấu trúc ảnh hưởng đến chức năng của các tương tác giữa các phân tử sinh học. Mặc dù những thay đổi về cấu trúc và động lực học có thể tinh vi và mặc dù chúng có thể yêu cầu các công cụ đo lường chuyên dụng cao, chúng làm nhiễu loạn một hệ thống cân bằng đủ để tạo điều kiện thuận lợi cho dịch bệnh.
Dựa trên việc xem xét các tài liệu và các suy luận dựa trên thực nghiệm mà chúng tôi đã đề xuất ở đây, chúng tôi khẳng định rằng các cụm nano có cấu trúc động của nước từ hóa cung cấp các khối xây dựng và các yếu tố chức năng thiết yếu trong hệ thống sống, và sự gián đoạn của chúng gây ra bệnh tật. Luận điểm của chúng tôi về cơ bản khác với luận điểm của Gryder, Nelson, và Shepard [349], ở chỗ cho rằng nước giao diện có cấu trúc tổ chức tất cả các quá trình lý sinh có khuôn mẫu cao về sự sống cơ bản. Trong khi Gryder et al. đã áp dụng tín điều trung tâm, SMT, cho giả thuyết entropy gen sinh học của Oller [1], luận án EIWS của chúng tôi ủng hộ và làm tăng thêm TOFT, như được thể hiện bởi Sonnenschein và Soto, loại bỏ gen khỏi ghế lái xe (thuyết xác định di truyền) và giới thiệu sinh vật và khả năng tự tổ chức của nó như là trọng tâm khái niệm (chủ nghĩa hữu cơ) của sinh học ung thư [293,295,350]. Năm 2004, Jones và cộng sự. lưu ý rằng tương tác của protein với một mảng lớn các polyanion được đặc trưng bởi mức độ đặc hiệu thấp hơn so với các tương tác đại phân tử được công nhận phổ biến nhất [351]. Để hỗ trợ cho luận điểm trọng tâm của bài báo của chúng tôi, chúng tôi đã trình bày chi tiết cách các HSPG (polyanions nội sinh phổ biến) và động lực nước hai mặt, khi bị EIWS phá vỡ, trong một quá trình đa kinh có thể dẫn đến ung thư và nhiều bệnh vô căn khác. bệnh của ngày nay.
Luận điểm trọng tâm của chúng tôi là bất kỳ thứ gì góp phần vào EIWS, bất kỳ thứ gì phá hủy các cụm nano của nước từ hóa, đều phải dẫn đến sự gia tăng entropi, “sự ngắn mạch”, giải phóng năng lượng của các điện thế màng, thúc đẩy phản ứng protein mở ra (UPR), Đáp ứng DNA (UDR), và quá trình chết rụng. Thật vậy, chúng tôi đề xuất rằng bất cứ thứ gì phá hủy nước giao thoa, gây nhạy cảm và thường gây ra một chuỗi phản ứng dây chuyền phân nhánh dẫn đến viêm nhiễm, bệnh tật và tử vong [2]. Một thông điệp sâu sắc về hy vọng hiện tồn tại rằng kiểu hình ung thư có thể được bình thường hóa. Bằng chứng cho điều này đến từ các nghiên cứu cho thấy ung thư vú xâm lấn được phát hiện trên màn hình đôi khi có thể thoái lui một cách tự nhiên mà không cần điều trị [352]. Thông điệp này được hỗ trợ bởi nhiều tài liệu trong bốn thập kỷ qua, hiện đã được xác nhận và củng cố thông qua việc sử dụng các công cụ cho phép các nhà nghiên cứu xác định rõ ràng các tế bào bình thường từng là tế bào ung thư [292]. Chúng tôi đề nghị rằng việc ngăn ngừa ung thư, nếu không phải là phương pháp chữa trị, bây giờ có thể thấy trước được. Hơn nữa, theo luận án TOFT và EIWS, nhiều bệnh, bao gồm cả bệnh truyền nhiễm và bệnh thần kinh, sẽ có thể phòng ngừa được, nếu không muốn nói là chữa được.
7. Kết luận
Chúng tôi đã trình bày một khung khái niệm mới, trong đó bệnh lý có thể bắt nguồn từ sự phá vỡ ban đầu cấu trúc mạch lạc của nước bởi những kích thích rất tinh vi. Bằng chứng nghiên cứu ủng hộ quan điểm rằng căng thẳng nước giao diện ngoại sinh – sự gia tăng quá mức sức căng nước giữa bề mặt sinh học gây ra bởi các chất độc hóa học và sinh học như, ví dụ, cation metalloneurotoxin Al ― là phương tiện và cơ sở chính của các thay đổi bệnh lý ngoại bào và nội bào dẫn đến ung thư, bệnh thần kinh và bệnh truyền nhiễm. Do đó, quan điểm của chúng tôi chủ yếu là quan điểm siêu phân tử / lý sinh về căn nguyên của ung thư và các bệnh khác. Theo luận điểm của chúng tôi, cả cấu trúc gen và cấu trúc protein đều phụ thuộc vào trạng thái lý sinh của nước giữa các mặt; do đó, cấu trúc phân tử sinh học phản ứng với các sự kiện siêu phân tử. Chức năng đề xuất của các cụm phân tử nano của nước kết dính trong đĩa CD nước được thảo luận. Giả thuyết được đưa ra rằng cation Al, chẳng hạn, gây “ngắn mạch” hiệu quả cho các động cơ nano kết hợp của các màng sinh học của chúng ta, phá vỡ đáng kể sự tiêu thụ entropy cấu trúc cân bằng tinh tế, cần thiết cho sự phân tách điện tích và truyền cả năng lượng và thông tin xuyên suốt phần thân. Sự gia tăng đồng thời của căng thẳng nước giữa các bề mặt và sự mềm của các mô, với sự gián đoạn liên quan của bộ xương tế bào, hiện đã được ghi nhận bằng nhiều phương thức quang phổ. Chúng tôi lập luận thêm rằng biosulfat có thể đóng một vai trò quan trọng trong việc duy trì các miền nguyên sinh dựa trên nước, duy trì hoạt động lành mạnh của các bào quan. Do đó, mô hình này là một mô hình cảm ứng ung thư siêu phân tử, trung mô và có khả năng biểu sinh, có thể đóng vai trò là một mô hình hữu ích để hiểu rõ hơn về nhiều bệnh vô căn và có thể do mãn kinh ngày nay, bao gồm cả các bệnh thần kinh và truyền nhiễm. Chúng tôi dự đoán và dự đoán rằng các giả thuyết được trình bày ở đây là có thể chứng minh được, cả về mặt lý thuyết và thực nghiệm.
Sự nhìn nhận
Các tác giả chân thành cảm ơn các cuộc thảo luận với George Czerlinski, Martin Gruebele, Martina Havenith và Nada Verdel. Các tác giả cũng biết ơn năm nhà phê bình ẩn danh, những người có những phân tích chu đáo đã góp phần đáng kể vào việc hoàn thiện bài báo này. Công trình này được tài trợ một phần bởi Quanta Computers, Đài Bắc, Đài Loan, dưới sự tài trợ của Dự án Qmulus.
Xung đột lợi ích
Các tác giả tuyên bố không có xung đột lợi ích.

